PIERWOTNE CHŁONIAKI SKÓRY
Chłoniaki pierwotne skóry to różnorodna grupa rzadkich chorób limfoproliferacyjnych wywodzących się z limfocytów T/NK lub B skóry. W tym poradniku postaramy się wyjaśnić Ci, na czym polega dokładnie Twoja choroba, jak leczymy dane podtypy chłoniaków skóry oraz jak dbać o skórę zmienioną chorobowo. Należy tu z całą mocą podkreślić, że chłoniaki skóry w większości mają indolentny - przewlekły - przebieg, tak jak nadciśnienie czy cukrzyca. Często wymagają jedynie okresowej terapii lub po intensywniejszym leczeniu stosowane są terapie podtrzymujące.
SKÓRA, CZYLI GDZIE ROZWIJA SIĘ CHOROBA
Skóra to największy narząd człowieka, ważący 6% masy całego ciała i zajmujący 1,6-2m2 powierzchni. To nie tylko pokrowiec, czy okładka dla narządów wewnętrznych. To narząd funkcjonujący w symbiozie z całym organizmem.
Klasyczna chemioterapia (gemcytabina, liposomalna doksorubicyna) jest rozważana dopiero po wyczerpaniu wyżej opisanych metod, dedykowanych do leczenia chłoniaków skóry.
Zmieniona skóra traci właściwości skutecznej bariery chroniącej nas przed infekcjami, więc dodatkowe obniżenie odporności, np. związane ze spadkiem liczby białych krwinek po każdym cyklu chemioterapii może prowadzić do poważnych powikłań infekcyjnych.
Większe ryzyko niesie polichemioterapia, która może być jedyną dostępną opcją leczenia w zaawansowanym stadium choroby. Stosujemy schematy takie, jak np.
- CHOP (Cyklofosfamid | Hydroxydaunomycyna – nazwa chemiczna doksorubicyny | Oncovin – jedna z nazwy winkrystyny | Prednizolon)
- EPOCH (Etopozyd | winkrystyna – Oncovin | doksorubicyna – Hydroxydaunomycyna | Cyklofosfamid),
- ESHAP (Etopozyd | Solumedrol – steryd – metyloprednizolon | HD-Ara-C | cisplatyna – zawiera Platynę)
W przypadku klasycznej chemioterapii należy jej potencjalne działania nie-pożądane omówić szczegółowo przed rozpoczęciem leczenia. Większość z nich występuje podczas podawania chemioterapii lub bezpośrednio po: nudności, osłabienie, utrata apetytu, łysienie, większa podatność na infekcje, ale część działań niepożądanych może ujawnić się dopiero po miesiącach lub latach (np. powikłania kardiologiczne lub neurologiczne związane z konkretnymi cytostatykami).
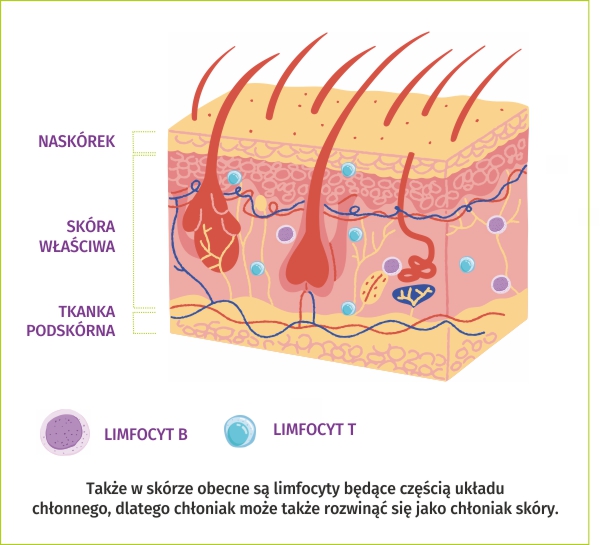
Skóra składa się z naskórka, skóry właściwej i tkanki podskórnej (tłuszczowej). Naskórek budują keratynocyty – ułożone jak cegiełki połączone pewnego rodzaju zaprawą (substancją międzykomórkową). W skórze spotkamy też melanocyty – odpowiadające za kolor naszej skóry, a także za ochronę przed promieniowaniem ultrafioletowym, adipocyty (komórki tkanki tłuszczowej), komórki dendrytyczne (Langerhansa), Merkla, fibroblasty, histiocyty, komórki tuczne i limfocyty.
Wszystkie one wspólnie utrzymują skórę w formie, stanowiąc wielozadaniową izolację. Skóra chroni nas przed zimnem, ciepłem, czynnikami chemicznymi, bakteriami, wirusami, przed utratą wody. Odpowiada za równowagę wodnoelektrolitową i termoregulację (jeżeli zmieniona jest duża powierzchnia skóry, dochodzi do zaburzeń termoregulacji, co może być przyczyną go-rączki, dreszczy). Skóra pozwala na odczuwanie dotyku, ciepła i zimna. Dzięki niej produkujemy witaminę D. Skóra bierze też udział w procesach immunologicznych i zapewnia odporność ustroju. Obecne w skórze limfocyty produkowane są w szpiku kostnym, a po modyfikacjach w grasicy i obwodowych narządach limfatycznych, strzegą zdrowia organizmu.
Limfocyty krążąc w organizmie, wspierają m.in. rozpoznawanie patogennych bakterii, wirusów, biorąc udział w ich zwalczaniu, a także wspierają walkę organizmu z nowotworami. Czasem jednak – tak jest w białaczkach i chłoniakach – same ulegają transformacji: limfocyt mutuje, dzieli się i namnaża, tworząc klon identycznych komórek nowotworowych.
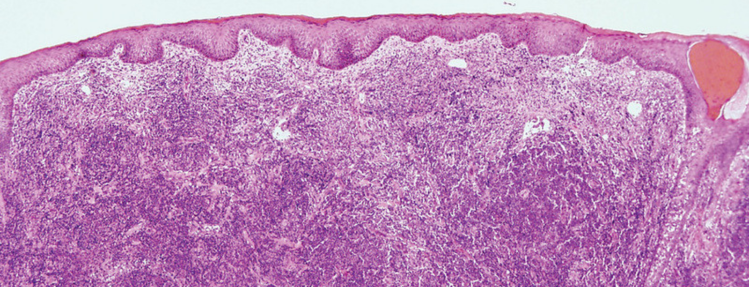
Proces ten może zajść w każdym narządzie w którym limfocyty są obecne – także w skórze. To dlatego można zachorować na chłoniaka rozwijającego się pierwotnie w skórze, gdzie monoklonalny naciek komórek nowotworowych namnaża się, zdobywa pewną autonomię i zaczyna niszczyć zdrową skórę.
Nie wiadomo do końca, co jest pierwotną przyczyną w danym, indywidualnym przypadku. Jednym z powodów, może być trwające długo pobudzenie limfocytów (tzw. stymulacja antygenowa) np. wywołane infekcją gronkowcem złocistym czy niektórymi lekami. Chłoniaki skóry obserwuje się częściej u osób z wrodzonym lub nabytym zespołem obniżonej odporności organizmu, niepozwalającym na w pełni skuteczne zwalczanie nowotworów na początku ich tworzenia.
Jako czynniki ryzyka uznaje się również palenie papierosów, prace w przemyśle drzewnym i rolnictwie oraz otyłość (wskaźnik BMI>30). Wskaźnik BMI to stosunek masy ciała (wagi) do wzrostu. Niskie wartości mówią o tym, że ważmy za mało, wysokie – że za dużo. Dorosły człowiek o prawidłowym stosunku wagi do wzrostu ma wskaźnik w granicach 18,5–24,9. Obliczenie wskaźnika BMI jest bardzo proste. Aby móc to zrobić, potrzebne są dwie dane: wzrost i aktualna masa ciała. Należy podzielić wagę wyrażoną w kilogramach przez wzrost podniesiony do kwadratu, wyrażony w metrach, czyli BMI = kg/m2.Można tez skorzystać z dostępnych w internecie kalkulatorów.a
DIAGNOSTYKA, CZYLI SKĄD WIEM, ŻE TO CHŁONIAK SKÓRY
Gdy lekarz podejrzewa chłoniaka skóry – będzie tak prowadził diagnostykę, aby potwierdzić sam fakt, że jest to chłoniak, a także określić jego podtyp. Ma to istotne znaczenie dla wyboru leczenia, prowadzonego w Polsce przez dermatologów, hematologów i onkologów, w tym specjalistów radioterapii.
Klasyczna chemioterapia (gemcytabina, liposomalna doksorubicyna) jest rozważana dopiero po wyczerpaniu wyżej opisanych metod, dedykowanych do leczenia chłoniaków skóry.
Zmieniona skóra traci właściwości skutecznej bariery chroniącej nas przed infekcjami, więc dodatkowe obniżenie odporności, np. związane ze spadkiem liczby białych krwinek po każdym cyklu chemioterapii może prowadzić do poważnych powikłań infekcyjnych.
Większe ryzyko niesie polichemioterapia, która może być jedyną dostępną opcją leczenia w zaawansowanym stadium choroby. Stosujemy schematy takie, jak np.
- CHOP (Cyklofosfamid | Hydroxydaunomycyna – nazwa chemiczna doksorubicyny | Oncovin – jedna z nazwy winkrystyny | Prednizolon)
- EPOCH (Etopozyd | winkrystyna – Oncovin | doksorubicyna – Hydroxydaunomycyna | Cyklofosfamid),
- ESHAP (Etopozyd | Solumedrol – steryd – metyloprednizolon | HD-Ara-C | cisplatyna – zawiera Platynę)
W przypadku klasycznej chemioterapii należy jej potencjalne działania nie-pożądane omówić szczegółowo przed rozpoczęciem leczenia. Większość z nich występuje podczas podawania chemioterapii lub bezpośrednio po: nudności, osłabienie, utrata apetytu, łysienie, większa podatność na infekcje, ale część działań niepożądanych może ujawnić się dopiero po miesiącach lub latach (np. powikłania kardiologiczne lub neurologiczne związane z konkretnymi cytostatykami).
W większości przypadków rozpoznanie pierwotnych chłoniaków skóry ustala dermatolog wraz z patomorfologiem (specjalistą oceniającym pod mikroskopem mały fragment pobranej od pacjenta biopsji skóry po jego odpowiednim zabarwieniu). We wczesnych stadiach choroby trudno jednoznacznie ocenić charakter nacieku ze względu na niewielką ilość klonu nowotworowego. To chyba jedyny proces nowotworowy, gdzie zda-nie patologa rzadko jest ostateczne, a szczególne znaczenie ma sformułowanie „przy zgodnych danych klinicznych”.
Biopsję skóry wykonuje się w znieczuleniu miejscowym, po podaniu w iniekcji środka znieczulającego: lekarz pobiera skalpelem mały wycinek skóry o średnicy 5-10 mm, następnie zszywa ranę lub zakłada opatrunek ze spongostanem („gąbeczką” hamującą krwawienie). Chociaż samo znieczulenie „nieco szczypie” i powoduje uczucie rozpierania, pozostała część procedury jest całkowicie niebolesna. Cały zabieg trwa najczęściej ok. 15 minut, z czego najwięcej czasu zajmuje omówienie z chorym, na czym on polega i założeniem opatrunku. Opatrunek warto pozostawić przez 1-2 doby, nie mocząc go, później trzeba zmieniać go codziennie, traktując miejsce biopsji jak skaleczenie (przemywając środkiem odkażającym, zakładając nowy jałowy gazik). Lekarz poinformuje, kiedy należy usunąć szwy, jeśli były zakładane (zaprosi do siebie lub pokieruje do ambulatorium chirurgicznego).
Pobrany fragment skóry jest wysyłany na tzw. badanie histopatologiczne do specjalisty patomorfologa. To on opisze, czy w przesłanym do badania materiale znalazł cechy chłoniaka czy nie, a jeśli tak to jaki to typ.
Oprócz klasycznej oceny morfologicznej pobranej tkanki, w razie podejrzenia chłoniaka, wykonuje się dodatkowe badania immunohistochemiczne, pozwalające na uwidocznienie znajdujących się na powierzchni komórek białek (antygenów), takich jak CD2 CD3, CD5, CD7, CD19, CD20, CD30, CD56, MUM1, Foxp3 i inne. Pozwalają one na określenie z jakich komórek składa się klon nowotworowy ( limfocytów T, B czy NK).
Te dodatkowe procedury wydłużają czas badania – stąd czas oczekiwania na wynik to ok. 3 tygodnie. Czasem dłużej, gdy wycinki trafią do ośrodka niespecjalizującego się w diagnostyce chłoniaków, który po wstępnej ocenie przesyła preparaty do ośrodków referencyjnych.
Ten czas oczekiwania nie ma w praktyce znaczenia dla przebiegu choroby w większości chłoniaków skóry, które cechują się powolnym przebiegiem i różnica kilku tygodni we wdrożeniu leczenia nie zmienia przebiegu choroby. W przypadku dokuczliwych objawów, takich jak np. świąd – lekarz po pobraniu wycinka, oczekując na wynik, może je niwelować lekami przeciwhistaminowymi, rzadziej niskimi dawkami glikokortykosteroidów.
Uwaga – podanie sterydów przed badaniem histopatologicznym silnie działa na komórki chłoniaka, utrudniając ich ocenę, co może skutkować koniecznością pobrania dodatkowych wycinków.
Patomorfolog opisuje obraz, który jest widoczny pod mikroskopem. Wynik nie zawsze jest jednoznaczny, bo obraz, szczególnie na wczesnym etapie choroby, może nie być dla niej typowy. Otrzymujemy wówczas informację, że obraz może odpowiadać chłoniakowi, ale wynik należy skonfrontować ze stanem skóry, co wykonuje dermatolog. To on ocenia, czy zmiany są rumieniowe, naciekowe, czy to grudki, guzki, guzy – i czy opis w wyniku badania histopatologicznego „pasuje” do stanu skóry. Ta niejednoznaczność wyniku histopatologicznego wynika z faktu, iż naciek – tworzący się na początku chłoniaka skóry – składa się z mieszaniny komórek zapalnych i nowotworowych. Komórki chłoniaka mogą być pojedyncze, wmieszane w utkanie skóry zdrowej / ewentualnie reagującej stanem zapalnym. Chociaż dermatolog pobiera biopsję ze skóry zmienionej chorobowo, z miejsca najbardziej reprezentatywnego, patomorfolog może nie znaleźć tam początkowo nielicznych komórek chłoniakowych.
Z tego powodu pobranie biopsji skóry musi być w niektórych przypadkach kilkukrotnie powtórzone.
Postawienie diagnozy może dodatkowo utrudniać wdrożone wcześniej leczenie objawowe (np. zmian skórnych przypominających zmiany wypryskowe, czy łuszczycowe). Jeśli jest to możliwe, należy – po porozumieniu z lekarzem -przerwać stosowanie leków antymitotycznych (hamujących podziały komórkowe) czy działających przeciwzapalnie na 2-3 tygodnie przed pobraniem wycinka.
Należy wcześniej jednoznacznie wykluczyć powiększenie węzłów chłonnych, których pobranie do badania może być konieczne (węzły chłonne mogą być powiększone zarówno w zaawansowanych przypadkach chłoniaka skóry, jak również niektóre chłoniaki rozwijające się pierwotnie w węzłach chłonnych mogą wtórnie zajmować skórę – co wymaga różnicowania i odmiennego leczenia).
Jeżeli choroba zajmuje węzły chłonne – zwłaszcza, gdy są one duże lub nie-typowe w obrazie USG – należy je również przebadać. Pacjent jest kierowany do chirurga: preferuje się pobieranie węzła w całości, tak aby patomorfolog mógł nie tylko ocenić obecność komórek chłoniaka, ale także określić charakter ich nacieku i zaburzenia architerktury węzła. Biopsja gruboigłowa powinna być wykonana tylko w sytuacji, gdy węzeł jest bardzo trudno dostępny. Zbadanie węzła chłonnego ma znaczenie w określaniu stadium zaawansowania choroby.
Dla oceny stadium zaawansowania klinicznego używamy systemu TNMB (ang. Tumor–Nodes–Metastasis–Blood). Ocenia się rodzaj ( rumienie, nacieki lub guzy ) i rozległość zmian skórnych, zajęcie okolicznych węzłów chłonnych, obecność odległych przerzutów i obecność komórek chłoniakowych we krwi.
TK / PET-TK
Wykonuje się badania obrazowe tj. tomografię komputerową (TK) głowy, szyi, klatki piersiowej, jamy brzusznej i miednicy mniejszej lub pozytonową tomografię emisyjną (PET-TK).
W części chłoniaków skóry nie dochodzi w ogóle do zajęcia narządów wewnętrznych (np. w lymphomatoid papulosis, LyP), w innych przypadkach zajmowane są one dopiero po latach choroby (np. w u chorych na ziarniniaka grzybiastego, mycosis fungoides, MF). Badania obrazowe są jednak zasadne także we wczesnych stadiach ze względu na możliwość współistnienia innych chorób, które mogę mieć wpływ na wybór metody leczenia i dalsze postępowanie.
Badania obrazowe są wykonywane także celem oceny skuteczności leczenia lub sprawdzenia, czy choroba nie progresuje.
W badaniu TK można uwidocznić powiększone węzły chłonne lub naciekanie narządów wewnętrznych przez komórki chłoniaka, natomiast w badaniu PET-TK oceniamy dodatkowo ich aktywność metaboliczną. Wykorzystywany jest tu fakt, że komórki nowotworowe potrzebują więcej glukozy niż otaczające je komórki zdrowe. Podaje się dożylnie glukozę znakowaną izotopem – komórki nowotworowe „pochłaniają jej” więcej niż tkanki zdrowe. W PET-TK widać miejsca, w których gromadzi się glukoza właśnie dzięki izotopowi – im więcej izotopu w danej okolicy, tym silniejszy sygnał i wyższy parametr SUV, opisywany w wynikach PET-TK. Jednak podobnie aktywne metabolicznie są komórki na-cieku zapalnego – z tego powodu PET-TK nie pozwala na różnicowanie aktywnej infekcji od ogniska chłoniaka (badanie powinno być wykonane po wykluczeniu infekcji).
BADANIE SZPIKU I KRWI
Badanie szpiku (biopsja aspiracyjna oraz trepanobiopsja) nie jest konieczne w większości chłoniaków skóry, ale zasadna jest ocena rozmazu i immunofenotypizacja krwi obwodowej (z tego powodu lekarz zleci badania krwi podczas diagnostyki). W przebiegu chłoniaków skóry wywodzących się z limfocytów T możliwe jest wysokie stężenie IgE całkowitego we krwi (zwykle < 1000), co u części pacjentów omyłkowo jest uznane za związane z alergią. O aktywności choroby może świadczyć wysoki poziom dehydrogenazy mleczanowej (LDH).
WYMAZY
W przypadku erytrodermii (stanu, w którym zaczerwienione jest ponad 80% powierzchni ciała) lekarz może pobrać wymazy ze skóry, nosa, krwi na badanie bakteriologiczne i rozważyć podanie antybiotyku.
We wszystkich podtypach chłoniaków skóry opisane badania są niezbędne do różnicowania choroby z chłoniakami wywodzącymi się z innych narządów ( np. węzłów chłonnych, śledziony) i wtórnie zajmujących skórę.
CO WARTO WIEDZIEĆ O LECZENIU CHŁONIAKA SKÓRY?
Lekarz wybierze metodę leczenia właściwą dla typu chłoniaka i stadium zaawansowania zgodnie z najnowszą wiedzą medyczną. Omówi przebieg leczenia, w tym czas trwania terapii oraz efekty jej działań niepożądanych. Przed leczeniem, zwłaszcza systemowym należy także przygotować organizm do podjęcia terapii.
Klasyczna chemioterapia (gemcytabina, liposomalna doksorubicyna) jest rozważana dopiero po wyczerpaniu wyżej opisanych metod, dedykowanych do leczenia chłoniaków skóry.
Zmieniona skóra traci właściwości skutecznej bariery chroniącej nas przed infekcjami, więc dodatkowe obniżenie odporności, np. związane ze spadkiem liczby białych krwinek po każdym cyklu chemioterapii może prowadzić do poważnych powikłań infekcyjnych.
Większe ryzyko niesie polichemioterapia, która może być jedyną dostępną opcją leczenia w zaawansowanym stadium choroby. Stosujemy schematy takie, jak np.
- CHOP (Cyklofosfamid | Hydroxydaunomycyna – nazwa chemiczna doksorubicyny | Oncovin – jedna z nazwy winkrystyny | Prednizolon)
- EPOCH (Etopozyd | winkrystyna – Oncovin | doksorubicyna – Hydroxydaunomycyna | Cyklofosfamid),
- ESHAP (Etopozyd | Solumedrol – steryd – metyloprednizolon | HD-Ara-C | cisplatyna – zawiera Platynę)
W przypadku klasycznej chemioterapii należy jej potencjalne działania nie-pożądane omówić szczegółowo przed rozpoczęciem leczenia. Większość z nich występuje podczas podawania chemioterapii lub bezpośrednio po: nudności, osłabienie, utrata apetytu, łysienie, większa podatność na infekcje, ale część działań niepożądanych może ujawnić się dopiero po miesiącach lub latach (np. powikłania kardiologiczne lub neurologiczne związane z konkretnymi cytostatykami).
1. Chłoniaki to choroby układu chłonnego odpowiadające za odporność organizmu. Może w ich przebiegu pojawić się spadek odporności. Warto rozważyć szczepienia – p/grypie (sezonowo), p/Streptococcus pneumoniae, p/półpaścowi, p/krztuścowi, p/COVID-19, p/WZW B (w zależności od poziomu przeciwciał u osób szczepionych i u wszystkich nieszczepionych). Jest to szczególnie ważne w przypadkach, gdy pacjent będzie wymagał systemowego leczenia obniżającego odporność (chemioterapii). Najlepiej zaszczepić się przynajmniej 2 tygodnie przed rozpoczęciem leczenia, ale jeśli to nie jest możliwe, w wyborze najkorzystniejszego momentu pomoże lekarza prowadzący.
2. Przed leczeniem należy zadbać o zęby. Konieczny jest przegląd stomatologiczny i sanacja uzębienia (każda zmiana ogniskowa może przy spadku odporności prowadzić do sepsy).
3. U kobiet wskazana jest wizyta u ginekologa celem wykluczenia infekcji i chorób współistniejących, które mogłyby mieć wpływ na wybór leczenia.
Przed wdrożeniem terapii lekarz omawia z pacjentem jej przebieg, częstotliwość związanych z leczeniem wizyt i wykonywania badań kontrolnych. Omawia również wpływ leczenia nie tylko na chorobę, ale także na Twój stan ogólny, w tym ew. powikłania, które w przypadku leczenia chłoniaków skóry najczęściej nie są uciążliwe, choć mogą wystąpić.
W poradni prowadzi się leczenie, gdy zalecone są:
- kremy lub maści glikokortykosteroidowe,
- fototerapia,
- metotreksat w tabletkach lub iniekcjach,
- interferon (w poradni onkologicznej lub hematologicznej),
- beksaroten (w poradniach z dostępem do programu lekowego B.66).
W oddziale dziennym lub stacjonarnym prowadzi się leczenie w przypadku:
- beksarotenu (ostatnio również w poradniach),
- brentuksymabu wedotyny,
- mogamulizumabu,
- chemioterapii,
- radioterapii,
- mechloretaminy, dostępnej jedynie w ramach procedury RDTL (Ratunkowy Dostęp do Technologii Lekowych).
Pobyt w oddziale dziennym trwa kilka godzin – to czas niezbędny dla przygo-towania leku przez aptekę szpitalną i jego podanie. Dodatkowo czas wydłuża oczekiwanie na – niezbędne dla bezpieczeństwa pacjenta – wyniki badań la-boratoryjnych (można to przyspieszyć wykonując badania 1-2 dni wcześniej). Na czas pobytu w oddziale dziennym warto uzbroić się w cierpliwość i zabrać ze sobą coś do czytania lub słuchania. Jeśli schemat leczenia wymaga kilku dni podawania leków – pobyt może potrwać kilka dni.

Zawsze należy informować lekarza o nowych lekach, zleconych z powodu innych chorób. W większości przypadków będzie je należało kontynuować, choć u części chorych będą konieczne modyfikacje.

Nie należy samowolnie wprowadzać ziół i suplementów – mogą one zaburzać wchłanianie leków przeciwnowotworo-wych, nasilać ich działania niepożądane, a nawet zmniejszać skuteczność leczenia chłoniaka
METODY LECZENIA CHŁONIAKÓW SKÓRY
W leczeniu chłoniaków skóry dysponujemy różnymi metodami, które dobierane są w zależności od danego podtypu, stopnia zaawansowania klinicznego oraz przebiegu choroby. Wśród nich znajdują się maści, kremy, leki stosowane doustnie czy podawane w postaci wlewów dożylnych, a także foto- czy radioterapia. W tym rozdziale opiszemy te metody.
Większość leków stosowanych w leczeniu chłoniaków skóry jest dobrze tolerowana, stąd dokuczliwe powikłania obserwujemy jedynie w nielicznych przypadkach. Jeśli to będzie zasadne, lekarz zleci badania krwi celem monitorowania wpływu leków na stan organizmu. W przypadku chłoniaków skóry wybór metody leczenia jest ściśle związany z typem chłoniaka – nie wszystkie z poniżej wymienionych leków są stosowane w każdym podtypie. Informacje o tym, które z poniższych leków mogą zostać zaproponowane konkretnie Tobie, znajdują się dalszej części poradnika przy omawianiu podtypów chłoniaków skóry.
Monoterapia z rytuksymabem, którą czasem pro-ponuje się pacjentom z małą masą guza, to zwy-kle 4 dawki podawane w odstępie tygodnia, z na-stępowym leczeniem podtrzymującym (dawki le-ku co 2-3 miesiące w kolejnych 2 latach).
GLIKOKORTKOSTEROIDY
W leczeniu chłoniaków skóry mogą być stosowane miejscowe maści i kremy z glikokortykosteroidami klasy I. Smaruje się nimi 1 raz dziennie i są stosowane dłużej niż zaleca ulotka leku – bo 3-4 miesiące.
Czasem są łączone z retinoidami miejscowymi, aby wzmóc działanie glikokortykosteroidów i jednocześnie zapobiec zanikowi skóry, który może wystąpić po przewlekłym stosowaniu glikokortykosteroidów miejscowo. Po posmarowaniu zmian chorobowych należy umyć ręce.
MECHLORETAMINA
Kolejny lek to mechloretamina w żelu – w Polsce dostępna na wniosek RDTL (Ratunkowy Dostęp do Technologii Lekowych), w ośrodkach, które mogą taki wniosek wystawić. Na świecie rekomendowana jest jako I lub II linia leczenia ziarniniaka grzybiastego. W Polsce możliwa do zalecenia po wyczerpaniu innych możliwości terapeutycznych dla danego stadium. Żel powinien być przewożony w coolerze, a więc warto się w taki zaopatrzyć.
Żel stosuje się raz dziennie w ilości 1 FTU (ang. fingertip unit) na aplikację – objętość produktu wyciśniętego z tuby na odcinek palca wskazującego od opuszka do pierwszego stawu międzypaliczkowego. Lek należy przechowywać w lodówce.
Podczas aplikowania mechloretaminy pacjenci i opiekunowie, jeśli pomagają pacjentowi nakładać lek, powinni stosować się do następujących instrukcji:
- Otwór tubki z żelem jest zabezpieczony foliową plombą. Do przekłucia plomby należy użyć zakrętki.
- Jeśli lek nakładasz sam, musisz dokładnie umyć ręce wodą z mydłem natychmiast po kontakcie z mechloretaminą lub po zaaplikowaniu produktu na obszary skóry dotknięte chorobą. W razie ekspozycji zdrowej skóry na mechloretaminę, nie denerwuj się, po prostu umyj ten obszar skóry wodą z mydłem.
- Jeśli smaruje Cię ktoś bliski – to musi stosować rękawice nitrylowe jednorazowego użytku. Po posmarowaniu musi je zdjąć, wywracając je na drugą stronę – w celu uniknięcia kontaktu z żelem – oraz dokładnie umyć ręce wodą z mydłem. Jeśli dojdzie do przypadkowego narażenia skóry opiekuna na mechloretaminę, musi on dokładnie umyć miejsca narażenia wodą z mydłem (przez co najmniej 15 minut) oraz ew. zdjąć i wyprać zanieczyszczoną odzież.
- Mechlroetaminę należy aplikować po wyjęciu z lodówki lub w ciągu 30 minut od wyjęcia. Tubkę należy chować do lodówki zaraz po każdora-zowym użyciu – włożyć czystymi rękami z powrotem do oryginalnego pudełka, a pudełko umieścić w dostarczonej przezroczystej zamykanej plastikowej torebce, przeznaczonej do przechowywania w lodówce.
- Mechloretaminę aplikuje się na całkowicie suchą skórę na co najmniej
4 godziny przed wzięciem prysznica lub myciem lub 30 minut po. - Należy odczekać 5 do 10 minut po aplikacji, aby leczone miejsca wyschły i dopiero potem nałożyć odzież. W miejscach na skórze, gdzie zaapliko-wano mechloretaminę, nie należy stosować opatrunku okluzyjnego (niedopuszczającego wilgoci ani powietrza). Jeśli natłuszczasz skórę balsamami – nałóż je na leczone miejsca na 2 godziny przed nałożeniem mechloretaminy lub 2 godziny po.
Z działań niepożądanych może wystąpić wyprysk, który najczęściej łatwo opanować, zmniejszając częstość aplikacji leku (nie codziennie tylko co 2-4 dni) i stosując go łącznie z miejscowymi steroidami.
Fototerapia (UVB lub nb-UVB, UVA1, PUVA) – wykonywana jest w placówkach dermatologicznych. Naświetlania odbywają się 3 razy w tygodniu przez co najmniej 3 miesiące.
Fototerapia może powodować oparzenie skóry (jak po długiej ekspozycji na promieniowanie słoneczne na plaży). Pacjent musi mieć możliwość kontaktu z lekarzem lub osobą naświetlającą, by móc zgłosić każdą infekcję lub zmiany w stosowanych lekach. Po naświetalniu skórę na-leży natłuścić i nawilżyć zalecanymi przez lekarza balsamami.
W przypadku wdrożenia PUVA będziesz musiał przyjmować tabletki uwrażliwiające skórę na UVA – po to, aby skrócić czas ekspozycji na to promieniowanie. Dawka jest dobierana do Twojej masy ciała.
Przyjmij tabletki godzinę przed naświetlaniem z posiłkiem lub popij tłustym mlekiem, aby uniknąć ew. dyskomfortu żołądkowego.
Po przyjęciu tabletek będziesz musiał chodzić do zachodu słońca w okularach przeciwsłonecznych chroniących Twoje oczy przed promieniowaniem UV.
Tabletek ani okularów nie stosuje się podczas naświetlań UVB.
Przeciwwskazaniem są m.in. wcześniejsze zachorowanie na czerniaka oraz zioła i leki powodujące fotonadwrażliwość (np. furosemid). Ponadto choroby tę nadwrażliwość powodujące (np. toczeń) oraz padaczka (na początku procedury lampy emitują błyski mogące prowokować napad padaczkowy).
Do leków powszechnie dostępnych należy metotreksat. Jest to lek przeciwnowotworowy i immunosupresyjny. Hamuje syntezę nukleotydów purynowych oraz tymidynianów niezbędnych do syntezy i naprawy DNA oraz replikacji komórkowej.
Dawki stosowane w chłoniakach skóry są najczęściej takie same jak u pacjentów z łuszczycą: 10-25 mg 1 raz w tygodniu. W przypadku tabletek dawkę często dzieli się na trzy – przyjmowane w odstępach 12-godzinnych, np. dawka 20 mg tygodniowo oznacza, iż możesz ją przyjmować w następujący sposób:

Oczywiście dni mogą być inne, ale zawsze co tydzień te same. Jeśli będziesz miał zalecony metotreksat w iniekcjach – będzie to 1 iniekcja raz w tygodniu (co 7 dni).
Konieczna jest okresowa kontrola badań krwi. Monitorujemy ALAT, ASPAT oce- niające stan wątroby; morfologię krwi obwodowej z rozmazem, aby sprawdzić, czy nie spada poziom Twoich leukocytów, erytrocytów lub płytek krwi oraz kreatyninę, której wyższy poziom może sprzyjać gorszej eliminacji leku,
a tym samym nasilać objawy niepożądane). Ponadto konieczna jest suplementacja kwasu foliowego, który należy przyjmować 1 raz w tygodniu mini-mum dobę po metotreksacie – nigdy razem. Podczas leczenia należy unikać picia alkoholu.
Metotreksat wchodzi w interakcje z licznymi lekami, np. niesteroidowymi przeciwzapalnymi tj. salicylany, niektórymi antybiotykami (penicyliny, sulfonamidy, tetracykliny), omeprazolem, niektórymi lekami moczopędnymi i innymi. Z tego powodu zanim rozpocznie się przyjmowanie nowych leków podczas kuracji metotreksatem – należy poinformować lekarza przepisującego nowe leki o przyjmowaniu metotreksatu, a jeśli chcemy zażyć lek bez recepty – należy skontaktować się z lekarzem, który przepisał metotreksat w celu omówienia ryzyka.
Interferon wykazuje działanie antyproliferacyjne (przeciwpodziałowe), wpływa na różnicowanie się komórek oraz działa stymulująco na układ immunologiczny.
Interferon alfa (i jego postać pegylowana) – do niedawna dostępny w Polsce w ośrodkach hematologicznych i onkologicznych, od września 2024 jedynie na wniosek o import docelowy lub wniosek w ramach procedury RDTL.
Interferon podaje się samodzielnie w domu, w iniekcjach 1 raz w tygodniu. Jeśli dostępne są postaci niepelgylowane interferonu (o krótszym czasie działania) – wówczas iniekcje należy przyjmować 3 razy w tygodniu.
W czasie leczenia interferonem konieczna jest regularna kontrola badań laboratoryjnych krwi. Monitorujemy m.in. ALAT, ASPAT – tzw. transaminazy, które m.in. świadczą o kondycji Twojej wątroby oraz morfologię krwi obwodowej z rozmazem – gdyż lek może obniżać liczbę Twoich komórek krwi – zarówno leukocytów, jak i erytrocytów oraz płytek krwi.
Bezpośrednio po podaniu leku można spodziewać się uczucia rozbicia, dreszczy, bólu mięśni, stawów i gorączki – jak podczas infekcji np. paragrypowej. Można tym objawom zapobiec, przyjmując paracetamol lub ibuprofen po iniekcji interferonu i np. przed snem.
U części chorych obserwuje się obniżenie nastroju, a nawet depresję. Nie ukrywaj tych objawów przed lekarzem. Można i należy w takich przypadkach skorzystać z pomocy psychia-try i rozważyć okresowe stosowanie leków antydepresyj-nych.
Kolejnym lekiem jest beksaroten (w tabletkach). Aktywność biologiczna beksarotenu wynika ze zdolności do selektywnego wiązania i aktywacji trzech receptorów RXR: alfa, beta i gamma. W wyniku aktywacji receptory funkcjonują jako czynniki transkrypcyjne regulujące szereg procesów ta-kich jak: różnicowanie i namnażanie komórek oraz apoptoza, tzn. zaprogramowana śmierć komórki.
Lek dostępny w Polsce w programie lekowym (B.66), wydawany jest pacjentowi nieodpłatnie w placówkach realizujących ten program NFZ.
Jego stosowanie prowadzi u niemal wszystkich pacjentów do podwyższenia poziomu trójglicerydów i cholesterolu we krwi. Z tego powodu przed rozpoczęciem leczenia beksarotenem włączane są leki hipolipemizujące.
Zalecana jest także dieta niskotłuszczowa – z ograniczeniem potraw smażonych i słodyczy; bardzo restrykcyjna u osób, które już wcześniej miały problem z cholesterolem.
Innym częstym działanie niepożądanym jest zaburzenie pracy tarczycy (poziom TSH spada – często prawie do 0 i pozostaje niski, pomimo prawidłostosowanej suplementacji hormonami tarczycy). Zalecane dawki hormonów tarczycowych są często wyższe niż w klasycznej niedoczynności tarczycy. Prawidłowość przyjmowanych dawek hormonów tarczycy monitoruje się, oceniając nie poziom TSH, a poziom trijodotyroniny (fT3) i wolnej frakcji tyroksyny ( fT4) we krwi.
Regularność wizyt i badań określona przez warunki programu lekowego pozwala na dobrą kontrolę parametrów krwi i szybkie reagowanie na nieprawidłowości. Niski poziom TSH jest powszechnie kojarzony z nadczynnością tarczycy, jednym z przeciwwskazań do podania kontrastu w czasie TK ( tomografii komputerowej). Tego typu niedoczynność tarczycy (z niskim poziomem TSH) jest mało znana, gdyż występuje bardzo rzadko. Niedoczynność tarczycy związana z beksarotenem nie jest przeciwwskazaniem do badania TK z kontrastem.
Z tego powodu, w razie potrzeby wykonania TK, powinno to być w jasny sposób napisane na skierowaniu, aby personel medyczny sprawdzający wyniki badań przed podaniem kontrastu – zobaczywszy niski poziom TSH, nie odstąpił
od badania.
Brentuksymab wedotyny to tzw. „celowana chemioterapia”, nowoczesne leczenie, w którym toksyna komórkowa (prowadząca do śmierci komórki nowotworowej), połączona jest z przeciwciałem monoklonalnym ukierun-kowanym przeciwko antygenowi CD30 (które łączy się z jednometylowaną aurystatyną E).
Dlatego jest to lek dla pacjentów, u których na powierzchni komórek chłoniaka potwierdzono obecność antygenu CD30. Ponieważ ekspresja tego antygenu na komórkach chłoniaka bywa różnorodna (u tego samego pacjenta w jednych zmianach można znaleźć ten antygen, a w innych nie) – czasem potrzeba pobrać w tym samym czasie kilka biopsji z różnych miejsc na skórze (minimum dwie), aby móc potwierdzić obecność tego antygenu.
Lek jest dostępny w programie lekowym B.66 i podawany we wlewach dożylnych co 3 tygodnie, najczęściej w warunkach oddziału dziennego (pobyt jednodniowy).
Prowadząc leczenie, w badaniach krwi kontroluje się parametry wątrobowe, czynność nerek i wydolność szpiku (badanie morfologii).
Należy zwrócić uwagę na pierwsze objawy polineuropatii (takie jak mrowie-nie palców rąk i stóp, mniejszą siłę mięśni ramion, rąk, nóg), które z czasem mogą prowadzić do problemów z utrzymaniem przedmiotów w ręce czy zaburzeń równowagi utrudniających chodzenie. Trzeba zgłosić te dolegliwości, gdy tylko się pojawią. Neuropatię można leczyć – są odpowiednie ćwiczenia i leki, a w niektórych przypadkach zmniejsza się dawkę brentuksymabu.
To kolejny lek dostępny w programie lekowym NFZ B.66. – przeciwciało przeciw receptorowi chemokinowemu CCR4. Bardzo skutecznie zmniejsza liczbę komórek chłoniaka we krwi (już po 2-3 miesiącach stosowania), prowadzi także do regresji zmian skórnych i powiększonych węzłów chłonnych (na odpowiedź na leczenie z tych narządów czeka się nieco dłużej).
Podawany we wlewie dożylnym raz w tygodniu w dniach 1, 8, 15 i 22 pierwszego cyklu trwającego 28 dni, a następnie co dwa tygodnie w dniach 1 i 15 każdego następnego 28-dniowego cyklu.
Z reguły jest dobrze tolerowany, może jednak powodować zmiany skórne typu wyprysku. Jeśli w czasie leczenia mogamulizumabem pojawią się nowe swędzące zmiany – lekarz może zdecydować o pobraniu biopsji skóry, aby stwierdzić czy to nie jest reakcja na lek. Udowodniono, że pojawienie się tej reakcji (zwanej MAR, ang. mogamulizumab adverse reaction) koreluje z dobrą odpowiedzią na leczenie. Lekarz pomoże Ci w uporaniu się z objawami MAR, które najczęściej nie są bardzo uciążliwe.
Klasyczna chemioterapia (gemcytabina, liposomalna doksorubicyna) jest rozważana dopiero po wyczerpaniu wyżej opisanych metod, dedykowanych do leczenia chłoniaków skóry.
Zmieniona skóra traci właściwości skutecznej bariery chroniącej nas przed infekcjami, więc dodatkowe obniżenie odporności, np. związane ze spadkiem liczby białych krwinek po każdym cyklu chemioterapii może prowadzić do poważnych powikłań infekcyjnych.
Większe ryzyko niesie polichemioterapia, która może być jedyną dostępną opcją leczenia w zaawansowanym stadium choroby. Stosujemy schematy takie, jak np.
- CHOP (Cyklofosfamid | Hydroxydaunomycyna – nazwa chemiczna doksorubicyny | Oncovin – jedna z nazwy winkrystyny | Prednizolon)
- EPOCH (Etopozyd | winkrystyna – Oncovin | doksorubicyna – Hydroxydaunomycyna | Cyklofosfamid),
- ESHAP (Etopozyd | Solumedrol – steryd – metyloprednizolon | HD-Ara-C | cisplatyna – zawiera Platynę)
W przypadku klasycznej chemioterapii należy jej potencjalne działania nie-pożądane omówić szczegółowo przed rozpoczęciem leczenia. Większość z nich występuje podczas podawania chemioterapii lub bezpośrednio po: nudności, osłabienie, utrata apetytu, łysienie, większa podatność na infekcje, ale część działań niepożądanych może ujawnić się dopiero po miesiącach lub latach (np. powikłania kardiologiczne lub neurologiczne związane z konkretnymi cytostatykami).
Radioterapia polega na zastosowaniu promieniowania na zmienione chorobowo miejsca. Promieniowanie to zabija komórki nowotworowe.
Procedura znajduje zastosowanie zarówno w stadiach wczesnych, gdy nie ustępują uporczywe zmiany rumieniowe czy naciekowe, jak i późniejszych, gdy np. pojawią się guzy, a także jako wspomaganie innych metod terapii, tzn. że można stosować radioterapię podczas przyjmowania niektórych leków systemowych.
W przypadku zmian skórnych coraz częściej stosuje się brachyterapię – to metoda polegająca na umieszczeniu źródeł promieniowania w obrębie zmiany nowotworowej, w jej bezpośrednim sąsiedztwie lub w miejscu, z którego zmiana została usunięta. Tkanka w miejscu wprowadzonego izotopu otrzymuje wysoką dawkę promieniowania, ale wysoki gradient (spadek dawki wprost proporcjonalny do kwadratu odległości od źródła promieniowania) powoduje, że tkanki zdrowe, położone dalej, zostają oszczędzone, co ogranicza odczyny popromienne wokół leczonej zmiany.
Warto porozmawiać przed leczeniem z onkologiem, jak będzie wyglądała procedura i czego spodziewać się po niej (jak szybko ustąpi zmiana chłoniakowa, czy będzie po niej rana wymagająca leczenia, czy też nie).
Ponieważ stosowane w chłoniakach skóry dawki są dużo niższe niż przy innych nowotworach – rzadko obserwuje się odczyny popromienne (w większości przypadków gojenie przebiega szybko, z niewielkim świądem).
W czasie radioterapii należy – o ile lekarz prowadzący nie zaleci inaczej – myć się ciepłą wodą i natłuszczać lub nawilżać skórę poddawaną zabiegom.
W części ośrodków pacjent poddawany radioterapii kilka dni może dojeżdżać z domu, jeśli mieszka w niedalekiej odległości od placówki, czasem musi pozostać na oddziale lub przebywa w hotelu (np. w Gdańsku – jest wyznaczony skromny hotel przy UCK refundowany przez NFZ).
Jeśli zmian rumieniowych i naciekowych jest dużo, można rozważyć napromienianie całego ciała elektronami (TSEBT, ang. total skin electron beam therapy). Metoda ta jest dostępna w Polsce w kilku ośrodkach (w Gliwicach, Szczecinie), do których przyjeżdżają pacjenci z całego kraju.
Do działań niepożądanych należą okresowa utrata włosów, podrażnienie skóry całego ciała i jej złuszczanie, które można opanować stosując odpowiednie balsamy i kremy.
W niektórych przypadkach – gdy choroba postępuje pomimo leczenia, ale pacjent jest w dobrym stanie ogólnym – lekarz może zaproponować allogeniczne przeszczepienie komórek macierzystych (allo-SCT ang. allo-stem cel transplantation).
To procedura, podczas której pacjent otrzymuje od innej osoby (zgodnego dawcy – osoby spokrewnionej lub znalezionej w rejestrze dawców) zdrowe komórki krwiotwórcze (komórki macierzyste). Wymieniamy układ immunologiczny na inny, całkowicie sprawny, co daje szanse na pozbycie się komórek chłoniakowych. Dla pełnej skuteczności potrzeba czasu, stąd metoda ta przynosi najlepsze rezultaty u chorych, u których udało się wcześniej – przynajmniej na pewien czas – zahamować proces nowotworowy. Procedura obarczona jest wysokim ryzykiem infekcji i innych poważnych powikłań, co wymaga hospitalizacji w warunkach pełnej izolacji pacjenta przez parę tygodni po przeszczepieniu (pacjent nie może być w tym czasie odwiedzany).
Duże doświadczenie ośrodków transplantologicznych stosujących tą me-todę w chłoniakach skóry sprawia, że efekty są równie dobre jak na świecie.
LECZENIE KONKRETNYCH CHŁONIAKÓW SKÓRY
Chłoniaki skóry, w zależności od podtypu, mają różny przebieg oraz są inaczej leczone. To ważne, aby dokładnie znać swoje rozpoznanie, zwłaszcza poszukując informacji lub dzieląc się swoimi doświadczeniami z innymi pacjentami. Ponadto przebieg nawet dokładnie tej samej choroby może być inny u każdego pacjenta, a także zależy od chorób współistniejących. Dlatego pamiętaj, że ścieżka leczenia będzie zawsze dopasowana do typu chłoniaka oraz Twojego stanu ogólnego.
Pierwotne chłoniaki skóry T-komórkowe
Monoterapia z rytuksymabem, którą czasem pro-ponuje się pacjentom z małą masą guza, to zwy-kle 4 dawki podawane w odstępie tygodnia, z na-stępowym leczeniem podtrzymującym (dawki le-ku co 2-3 miesiące w kolejnych 2 latach).
ZIARNINIAK GRZYBIASTY ang. mycosis fungoides, MF
Jest to najczęściej występujący chłoniak skóry o licznych podtypach klinicznych.
- Najczęściej charakteryzuje się łagodnym wieloletnim przebiegiem, co nie oznacza, że nie potrafi dokuczyć ze względu na świąd skóry występujący u ok. 60-80% pacjentów.
- Zmiany mogą być rumieniowe, przebarwione, odbarwione, naciekowe (wypukłe), grudkowe, a w późnych stadiach choroby guzowate.
- Na powierzchni guzów mogą tworzyć się rany (płytkie nadżerki i głębsze owrzodzenia).
- Zmiany skórne mogą być pojedyncze (najczęściej wówczas zajmują obszary nieeksponowane na światło słoneczne tzn. doły pachowe, pośladki, biodra i pachwiny) lub liczne.
- Typowe jest współwystępowanie na skórze, w miarę postępu choroby, różnych rodzajów wykwitów.
Rokowanie u pacjentów z MF zależy od stadium w którym stawiana jest diagnoza (np. w stadium wczesnym, ze zmianami skórnym rumieniowymi i/lub naciekowymi, które nie przekraczają 10% powierzchni ciała 10 lat przeżywa ok. 98% pacjentów) oraz podtypu. Dobrze rokują odmiany MF typu siatkowicy pagetoidalnej, ziarniniakowatej obwisłości skóry (ang. granulomatous slack skin), nie tak dobrze rokują podtyp folikulotropowy czy z transformacją wielkokomórkową CD30+.
ZESPÓŁ SEZARY’EGO ang. Sezary syndrome, SS
U większości chorych z zespołem Sezary’ego można stwierdzić:
- Erytrodermię (początkowo zmiany przypominają wyprysk alergiczny, z czasem skóra staje się grubsza, nacieczona, twardsza, czerwonosina, złuszcza się, bardzo swędzi).
- Powiększone węzły chłonne (wyczuwalne dotykiem i widoczne w badaniach obrazowych na szyi, w dołach pachowych czy pachwinach).
- Obecność atypowych limfocytów T w skórze, węzłach chłonnych i krwi obwodowej (co można potwierdzić tylko badaniami).
- Inne objawy to: łysienie, pogrubienie i zniszczenie płytek paznokci, pogrubienie skóry (hiperkeratoza) dłoni i podeszew stóp.
Zgodnie z kryteriami ISCL (Międzynarodowego Towarzystwa Chłoniaków Skóry, ang. International Society of Cutaneous Lymphoma), aby rozpoznać SS, musi być też spełnione przynajmniej jedno z poniższych kryteriów:
- Bezwzględna liczba komórek Sezary`ego minimum 1000/mm3 krwi obwodowej.
- Zaburzenie proporcji limfocytów CD4:CD8 (wynik powyżej 10) i/lub utrata antygenów typowych dla limfocytów T (CD2, CD3, CD4, CD5, CD7, CD26), jednak nie zawsze to kryterium musi być spełnione.
- Wykazanie klonalności limfocytów T we krwi obwodowej za pomocą metod molekularnych lub cytogenetycznych.
Rokowanie jest poważniejsze niż w ziarniniaku grzybiastym – choroba wymaga szybkiego wdrożenia leczenia systemowego.
LECZENIE
ZIARNINIAKA GRZYBIASTEGO i ZESPOŁU SEZARY’EGO
Celem leczenia MF/SS jest ustąpienie lub zmniejszenie nasilenia objawów i stabilizacja choroby, zminimalizowanie ryzyka progresji oraz poprawa jakości życia.
Wybór terapii ziarniniaka grzybiastego zależy jest od stadium choroby, przy czym zasadą jest wstępne leczenie najlepiej tolerowanymi schematami terapeutycznymi, obejmujące terapie ukierunkowane na skórę (SDT, ang. skin directed therapies) czy wybrane leki systemowe (działające w całym organizmie). Dopiero w razie braku ich skuteczności rozważa się zastosowanie innych opcji leczenia, które niosą ze sobą większe ryzyko działań niepożądanych i immunosupresji (obniżenia odporności) np. chemioterapii. Część metod leczenia jest stosowana do uzyskania remisji, inne są kontynuowane jako terapia podtrzymująca celem utrzymania kontroli choroby. Trzeba uzbroić się w cierpliwość, ponieważ na zadowalającą poprawę podczas leczenia MF trzeba często czekać ok. 3-4 miesięcy.
MAŚCI I KREMY, FOTOTERAPIA, BRACHYTERAPIA
Wczesne stadia zaawansowania MF leczone są głównie przez dermatologów z wykorzystaniem terapii SDT, takich jak miejscowe maści i kremy z glikokortykosteroidami klasy I, mechloretamina w żelu, fototerapia czy rzadziej brachyterapia.
IMIKWIMOD
Można zastosować również imikwimod, który jest zarejestrowany do leczenia innych chorób, ale zgodnie z rekomendacjami – stosowany również w MF. Lek powoduje odczyn zapalny skóry, czasem pojawiają się nadżerki. Te objawy występują często, więc lekarz uprzedzi o ich wystąpieniu i przekaże zalecenia, jak łagodzić tę dolegliwość, stosując odpowiednie kremy.
LEKI SYSTEMOWE
W przypadku niezadawalającej odpowiedzi na leczenie SDT lub rozległego zajęcia skóry, w razie pojawienia się guzów, zajęcia krwi obwodowej czy pewnych podtypów chłoniaka (np. postaci folikulotropowej, postaci z tran-sformacją wielkokomórkową CD30+), SDT można łączyć z lekami systemowymi (czyli działającymi w całym organizmie chorego). Wówczas terapia może obejmować metotreksat, interferon alfa, beksaroten, brentuksymab wedotyny, mogamulizumab, a w przypadku wyczerpania opisanych metod leczenia włącza się klasyczną chemioterapię.
Podczas leczenia lekarz będzie Ci zlecał badania krwi i badania obrazowe – kontrolując bezpieczeństwo terapii. Badania są wykonywane również dlatego, że z ziarniniakiem grzybiastym mogą współistnieć inne choroby, których wystąpienie może mieć znaczenie np. dla wyboru kolejnej metody leczenia.
W przypadku zespołu Sezary’ego, zgodnie z rekomendacjami, leczeniem pierwszego rzutu powinna być fotofereza pozaustrojowa (ECP, ang. extra-corporeal photopheresis). Jednak z powodu braku refundacji w Polsce wykonywana jest u chorych na chłoniaka skóry tylko w nielicznych ośrodkach. ECP może być kojarzona z lekami systemowymi. ECP znajduje też zastosowanie w MF z zajęciem krwi obwodowej. Stosowana jest również w przypadku wystąpienia reakcji skórnej przeciw gospodarzowi po allogenicznym przeszczepieniu komórek macierzystych. W zespole Sezary’ego zastosowanie znajdują też leki systemowe tj. mogamulizumab oraz beksaroten (dostępne w programie lekowym B.66), interferon i inne.
U pacjentów z SS i z MF w zaawansowanym stadium, w dobrym stanie ogólnym, bez dobrej, długotrwałej odpowiedzi na wcześniej stosowane metody leczenia, można rozważyć allogeniczne przeszczepienie komórek macierzystych allo-SCT (ang. allogeneic stem cell transplantation). Najlepiej odpo-wiadają pacjenci, którzy w chwili przeszczepu są (dzięki innym metodom terapii) w całkowitej remisji choroby.
Na świecie dostępne są też inne metody leczenia – z zastosowaniem m.in. przeciwciał monoklonalnych, inhibitorów deacetylazy histonowej (HDAC), nowych antagonistów kwasu foliowego. Worinostat i romidepsyna, pralatreksat, alemtuzumab są metodami terapii systemowej o różnej, ale potwierdzonej skuteczności w zaawansowanych stadiach MF oraz w SS – niestety w Polsce nie są jeszcze dostępne.
Przyszłością MF i SS opornych na leczenie może być immunoterapia np. inhibitory PD-1 – pembrolizumab. W toku są badania klinicznie z lekami duvelisib z nivolumabem, ibrutynibem, resimune (anty-CD3), humanizowanym przeciwciałem indukującym cytotoksyczność anty-KIR3DL2.
Lekarz może zaproponować pacjentowi udział w badaniu klinicznym, które zapewni nieodpłatny dostęp do nowych technologii medycznych. Jest to kolejna opcja terapeutyczna warta rozważenia na każdym etapie choroby.
Warto z lekarzem omówić za i przeciw. Udział w badaniu klinicznym jest dobrowolny. Po rozpoczęciu leczenia w badaniu zawsze można zrezygnować z udziału. W trakcie badania klinicznego pacjent jest dokładnie i regularnie badany ( w tym ma wykonywane badania krwi, badania obrazowe – zgodnie z protokołem badania), a więc pozostaje pod dobrą opieką.
GRUDKOWATOŚĆ LIMFOIDALNA ang. lymphomatoid papulosis, LyP
LyP to przewlekła, nawracająca choroba dotykająca zarówno dzieci, jak i dorosłych, o charakterystycznym obrazie klinicznym:
Na skórze pojawiają się okresowo wspomniane już grudki z niewielkim złuszczaniem, czasem z powierzchownym owrzodzeniem. Grudki mogą samoistnie zanikać w ciągu 3–12 tygodni, by później pojawić się znów. U części pacjentów odstępy między kolejnymi wysiewami grudek trwają wiele miesięcy, u innych nowe zmiany pojawiają się już w czasie ustępowania tych z poprzedniego wysiewu.
Rozpoznanie histopatologiczne może sugerować innego chłoniaka, dlatego w LyP kluczowa do rozpoznania jest korelacja obrazu klinicznego z cechami histopatologicznymi biopsji skóry, ponieważ wynik badania histopatologicznego może być taki sam, jak w typowym MF, chłoniaku anaplastycznym CD30+, chłoniaku Hodgkina, chłoniaku epidermotropowym CD8+ lub chło-niaku NK/Tkomórkowym. Nie wolno leczyć „wyniku badania histopatologicznego”! Jeśli zmiany skórne to grudki i guzki, które mają tendencje do samoistnego ustępowania i nawrotów – to najprawdopodobniej jest to LyP,pomimo iż wynik badania h istopatologicznego przemawia za innym typem nowotworu.
LyP ma bardzo dobre rokowanie (5-letnie przeżycie 100%) – pomimo braku możliwości wyleczenia. Choroba nie zajmuje krwi ani narządów wewnętrznych. Jednak u części chorych współistnieją inne nowotwory układu chłonnego, najczęściej o typie chłoniaka anaplastycznego z dużych komórek (pc-ALCL, anaplastic large cell lymphoma), MF, chłoniaka Hodgkina (HL, ang. Hodgkin lymphoma) lub chłoniaka niezarniczego (NHL, ang. non-Hodgkin lymphoma). Z tego względu chorzy na LyP powinni być regularnie badani. Nie ma ustalonej częstotliwości badań obrazowych i badań krwi – decyduje stan pacjenta i ewentualne objawy subiektywne.
LECZENIE LyP
LyP nie wymaga, ale może być leczona. Terapia nie ma wpływu na całkowite przeżycie i rokowanie. Jej zadaniem jest zniwelowanie objawów, co może być istotne, zwłaszcza gdy zmianom towarzyszy nasilony świąd. Zmiany mogą być zlokalizowane w miejscach widocznych (twarz, ręce) – co krępuje pacjentów i utrudnia im codzienne funkcjonowanie.
Można stosować miejscowe maści i kremy glikokortykosterydowe, foto-terapię lub metotreksat 1 raz w tygodniu w dawkach najczęściej niższych niż w łuszczycy (z suplementacją kwasu foliowego raz w tygodniu, dzień po metotreksacie). Pojedyncze zmiany oporne na leczenie, szczególnie te o średnicy przekraczającej 2 cm, można usunąć chirurgicznie lub poddać radioterapii.
PIERWOTNY CHŁONIAK ANAPLASTYCZNY SKÓRY Z DUŻYCH KOMÓREK CD30+
znany też jako: pierwotnie skórny chłoniak anaplastyczny z dużych komórek CD30+
ang. primary cutaneous anaplastic large cell lymphoma, PC-ALCL, CALCL
PC-ALCL dotyczy częściej dorosłych mężczyzn. Typowe dla choroby są pojedyncze (u 80% pacjentów ) lub liczne guzy o średnicy od 1 do 10 cm.
Guzy mogą ustępować samoistnie – ma to miejsce w ok 30% przypadków. Obraz histopatologiczny wycinka skóry jest jednoznaczny i pozwala na postawienie diagnozy. Tylko u około 10% chorych chłoniak zajmuje węzły chłonne. Lekarz zawsze musi wykluczyć możliwość wtórnego zajęcie skóry przez układową postać ALCL, chłoniaka Hodgkina lub MF CD30+, wykonując stosowne ku temu badania (np. TK lub PET-TK i pobranie węzła chłonnego do badania histopatologicznego).
LECZENIE PC-ALCL
W PC-ALCL w przypadku pojedynczego guza – należy go usunąć chirurgicznie lub poddać radioterapii z ok 2-centymetrowym marginesem skóry nie-zmienionej wokół guza. Całkowite remisje osiąga się w 95% przypadków.
Gdy zmiany są liczne zalecany jest metotreksat 1 raz w tygodniu w dawce jak w łuszczycy lub pegylowny IFN lub beksaroten (nie w Polsce z powodu programu lekowego, który nie uwzględnia beskarotenu w portfolio leków dla PC-ALCL). Po osiągnięciu remisji choroby leczenie można stopniowo odsta-wiać i zwykle nie obserwuje się nawrotów.
W przypadku braku odpowiedzi lub nawrotu po 1 terapii systemowej należy rozważyć bretnuksymab wedotyny w monoterapii lub z radioterapią miejscową. Polichemioterapia stanowi ostatni wybór. W zmianach zlokalizowanych (ograniczonych do jednego miejsca na skórze) rokowanie jest najczęściej bardzo dobre i agresywne leczenie nie jest konieczne.
CHŁONIAK PIERWOTNY SKÓRY T-KOMÓRKOWY TYPU ZAPALENIA TKANKI PODSKÓRNEJ
znany także jako: pierwotnie skórny chłoniak T-komórkowy typu zapalenia tkanki podskórnej
ang. subcutaneous panniculitis-like T-cell lymphoma, SPTCL
SPTCL jest rzadkim nowotworem dorosłych i dzieci, występujący z taką samą częstością u obu płci.
W chorobie występują pojedyncze lub mnogie guzy i/lub nacieki typu zapalenia tkanki podskórnej w obrębie kończyn i tułowia (widoczne i wyczuwalne dotykiem jako wypukłości skóry barwy sinawej lub różowo-beżowej).
Zmianom skórnym może towarzyszyć: podwyższona temperatura ciała, uczucie zmęczenia, utrata masy ciała, cytopenia (obniżony poziom białych krwinek, płytek lub erytrocytów we krwi obwodowej) oraz wzrost aktywności enzymów wątrobowych (transaminaz ASPAT, ALAT). SPTCL z reguły przebiega łagodnie, ale może być powikłany zespołem hemofagocytarnym (HPS, ang. hemophagocytic syndrome), co pogarsza rokowanie. Z tego powodu złe samopoczucie powinno być zawsze zgłaszane lekarzowi prowadzącemu.
Rozpoznanie jest możliwe w oparciu o wynik badania histopatologicznego, obraz kliniczny (zmiany skórne) i wyniki badań obrazowych, których wyko-nanie jest konieczne.
Trudności diagnostyczne sprawia różnicowanie z głęboką postacią tocznia
rumieniowatego (chorobą autoimmunologiczną) – dlatego potrzebna jest czasem współpraca dermatologa lub hematologa z reumatologiem.
LECZENIE SPTCL
Praktycznie zawsze stosuje się doustne glikokortykosteroidy (prednizon), – a gdy nie są skuteczne – w skojarzeniu z małymi dawkami metotrkesatu, beksarotenu (w Polsce niemożliwe, z powodu zapisów programu lekowego) lub cyklosporyny. Ostatni schemat jest dyskusyjny ze względu na potencjał prolimfoproliferacyjny leku: sama cyklosporyna przy przewlekłym stosowaniu może promować rozwój chłoniaka.
W przypadku zespołu hemofagocytarnego konieczne może być zastosowanie leczenia hematologicznego takiego, jak w agresywnych chłoniakach z dojrzałych komórek T: chemioterapii (CHOP) i/lub radioterapii.
W przypadkach z HPS opornych na CHOP znajdują zastosowanie inne leki z grupy chemioterapeutyków: kladrybina, DHAP, ESHAP, FLAG, mini-BEAM oraz allo-SCT.
- DHAP (Deksametazon (steryd) | High-dose (HD) cytarabina
(zwana Ara-C) | cisplatyna – zawiera Platynę) - FLAG (Fludarabina | HD-Ara-C | idarubicyna | G-CSF)
- ESHAP (Etopozyd | Solumedrol – steryd – metyloprednizolon |HD-Ara-C | cisplatyna – zawiera Platynę)
- mini-BEAM (karmustyna zwana BiCNU | Etopozyd | cytarabina (zwana Ara-C) | Melfalan)
Ze względu na brak badań klinicznych i prac dotyczących dużych grupy pacjentów – zalecenia diagnostyczno – terapeutyczne obejmują postępowanie oparte o małe grupy pacjentów lub wręcz pojedyncze przypadki opisane w piśmiennictwie.
Postępowanie zależy od oceny przebiegu klinicznego i podtypu chłoniaka. Chłoniaki o dobrym rokowaniu są leczone najczęściej miejscowo, chirurgicznie, ew. metodą radioterapii, choroby o agresywnym przebiegu są leczone systemowo w sposób podobny do terapii innych chłoniaków T komórkowych.
PIERWOTNA CHOROBA LIMFOPROLIFERACYJNA SKÓRYZ MAŁYCH I ŚREDNICH KOMÓREK T CD4+
znana także jako: pierwotnie skórna choroba limfoproliferacyjna z małych i średnich komórek T CD4+
ang. primary cutaneous CD4-positive small/medium T-cell lymphoproliferative disorder
To chłoniak o łagodnym przebiegu (5-letnie przeżycie 100%), w którym wy-stępują pojedyncze nacieki lub guzki, zwykle na twarzy / szyi / górnej części tułowia, bez zajęcia narządów wewnętrznych.
Diagnozę można postawić tylko przy nieobecności (także w wywiadzie) cech typowych dla ziarniniaka grzybiastego i typowego obrazu histopatologicznego wycinka skóry. Leczenie obejmuje wycięcie chirurgiczne, radioterapię miejscową lub doogniskowo podawane steroidy. Zmiany czasem ulegają samoistnej regresji po biopsji i nie wymagają leczenia.
PIERWOTNY CHŁONIAK SKÓRY Z KOMÓREK CD8+, akralny
znany także jako: pierwotnie skórny chłoniak z komórek T CD8+, akralny
ang. primary cutaneous acral CD8+ T-cell lymphoma, PCA-TCL
Chłoniak ten ma łagodny przebieg (rokowanie jest bardzo dobre, 5-letnie przeżycie 100%) – zajmuje stopy, dłonie, małżowiny uszne lub nos, na których pojawia się wolno rosnąca grudka lub guzek ( w jednym miejscu).
Rozpoznanie stawia się w oparciu o wynik histopatologiczny wycinka skóry. Nie ma konieczności badań obrazowych (choroba nie zajmuje narządów wewnętrznych). W leczeniu stosuje się miejscowe lub doogniskowe glikokortykosteroidy, usunięcie chirurgiczne lub radioterapię.
PIERWOTNY AGRESYWNY CHŁONIAK EPIDERMOTROPOWY SKÓRY Z CYTOTOKSYCZNYCH KOMÓREK T CD8+
znany także jako: pierwotnie skórny chłoniak epidermotropowy z cytotoksycznych komórek T CD8+
ang. primary cutaneous CD8-positive aggressive epidermotropic
cytotoxic T-cell lymphoma, AECTCL
W AECTCL grudki, guzki i guzy często z centralną martwicą i tworzącymi się owrzodzeniami (ranami) występują na ograniczonym obszarze lub są rozsiane. Nacieki chłoniakowe stwierdza się również w płucach, jądrach, ośrodkowym układzie nerwowym (OUN), na śluzówkach jamy ustnej, ale węzły chłonne nie są zwykle zajęte.
Chłoniak wymaga intensywnego leczenia hematologicznego. Rozpoznanie stawiane jest w oparciu o wynik badania histopatologicznego, konieczne są badania obrazowe (TK, PET-TK). W leczeniu większość ośrodków stosuje polichemioterapię w połączeniu z radioterapią. U młodych chorych i pacjentów w dobrym stanie ogólnym należy rozważyć przeszczepienie komórek macierzystych (allo-SCT).
PIERWOTNY CHŁONIAK SKÓRY Z KOMÓREK T GAMMA/DELTA
znany także jako: pierwotnie skórny chłoniak z komórek T gamma/delta
ang. primary cutaneous gamma/delta T-cell lymphoma, PCGD-TCL
PCGD-TCL klinicznie charakteryzuje się rozsianymi (głównie na kończynach) naciekami i/lub grudkami oraz wrzodziejącymi guzkami z ranami na powierzchni. U połowy pacjentów obserwuje się zajęcie błon śluzowych i narządów wewnętrznych, ale rzadko zajęte są węzły chłonne, śledziona lub szpik kostny.
Pacjent wymaga intensywnego leczenia hematologicznego. Rozpoznanie opiera się o wyniki badania histopatologicznego i badań obrazowych TK lub PET-TK. Z powodu bardzo rzadkiego występowania choroby – nie jest jednoznacznie określone optymalne leczenie. Najczęściej stosuje się wielolekową chemioterapię w połączeniu z radioterapią pojedynczych zmian. U młodych chorych w dobrym stanie ogólnym należy rozważyć przeszczepienie komórek macierzystych (allo-SCT).
Pierwotne chłoniaki skóry B-komórkowe
Klasyfikacja chłoniaków ulega stałym modyfikacjom. Klasycznie wyróżniano trzy podtypy pierwotnych chłoniaków skóry B- komórkowych.
Rozpoznanie jest stawiane w oparciu o wynik badania histopatologicznego wycinka skóry (biopsję pobiera dermatolog lub chirurg) ze szczegółowymi barwieniami immunohistochemicznym w kierunku CD10, CD19, CD20, MUM1, FoxP3, Bcl2, Bcl6 i innych. Obecność (oznaczana w wyniku+) lub brak (oznaczany -) konkretnych antygenów powierzchniowych na chłoniakowych limfocytach B przemawia za odpowiednim podtypem B-komórkowego chłoniaka skóry.
Konieczne jest wykonanie badań obrazowych TK lub PET-TK, badania krwi obwodowej / szpiku – celem potwierdzenia, że chłoniak wywodzi się ze skóry, a nie jest to wtórne zajęcie skóry w przebiegu chłoniaka wywodzącego się z narządów wewnętrznych. Leczenie prowadzi w większości przypadków hematolog we współpracy z onkologiem specjalistą radioterapii, z tego powodu po postawieniu diagnozy pacjent jest kierowany do w/w specjalistów.
Monoterapia z rytuksymabem, którą czasem pro-ponuje się pacjentom z małą masą guza, to zwy-kle 4 dawki podawane w odstępie tygodnia, z na-stępowym leczeniem podtrzymującym (dawki le-ku co 2-3 miesiące w kolejnych 2 latach).
Pierwotny chłoniak skóry strefy brzeżnej
znany także jako: pierwotnie skórny chłoniak strefy brzeżnej
ang. primary cutaneous marginal zone lymphoma, PCMZL
Gdy zmiany są pojedyncze zastosowanie znajduje radioterapia lub wycięcie chirurgiczne. Rekomendowane są też glikokortykosteroidy podane doogniskowo (u dermatologa).
W wybranych przypadkach (gdy zmiany są pojedyncze, nie sprawiają dolegliwości), można pozostawić je bez leczenia, ale pod czujną obserwacją lekarza. U pacjentów z towarzyszącą infekcją Borrelia burgdorferi należy wdrożyć celowaną antybiotykoterapię (można również u dermatologa).
W przypadku pacjentów z wieloogniskowymi zmianami skórnymi znajduje zastosowanie rytuksymab, chlorambucyl, IFN (u hematologa).
Pierwotny chłoniak skóry z ośrodków rozmnażania
znany także jako: pierwotnie skórny chłoniak z ośrodków rozmnażania
ang. primary cutaneous follicle centre lymphoma, PCFCL
Gdy zmiany są pojedyncze – wskazane jest usunięcie chirurgiczne lub radioterapia (u onkologa specjalisty radioterapii) – stosowana także, gdy zmiany są liczne (wówczas konieczne jest kilka serii radioterapii). U chorych z rozległym zajęciem skóry stosuje się rytuksymab w monoterapii (u hematologa). Nawroty (u ok 1/3 pacjentów) są zwykle ograniczone do skóry i można zastosować ponownie poprzednią metodą leczenia.
Pierwotny chłoniak skóry z dużych komórek B, typu kończynowego
znany także jako: pierwotnie skórny chłoniak z dużych komórek B, typu kończynowego
ang. primary cutaneous diffuse large B-cell lymphoma, leg type, PCDLBCL, LT
Przebieg tego chłoniaka jest bardziej agresywny, podobny do postaci narządowej chłoniaka rozlanego z dużych komórek B (DLBCL, ang. diffuse large B-cell lymphoma). Lekarzem prowadzącym pacjenta powinien być hematolog współpracujący z onkologiem specjalistą radioterapii.
W leczeniu tych pacjentów stosuje się immunochemioterapię wg programu R-CHOP (rytuksymab, cyklofosfamid, doksorubicyna, winkrystyna, prednizon), w wybranych przypadkach wraz z uzupełniającą radioterapią miejscową (z marginesem wokół zmiany 1-2 cm). Sama radioterapia jest postępowaniem z wyboru u osób, które nie kwalifikują się do chemioterapii np. z powodu stanu ogólnego, choć przynajmniej u części chorych można wtedy za-stosować rytuksymab w monoterapii. Na świecie zastosowanie znajdują również: dacetuzumab (przeciwciało anty CD40), inhibitory punktu kontrolnego: anty-PD1, anty-PDL-1, inhibitor kinazy tyrozynowej Brutona oraz lenalidomid.
Wrzody śluzówkowo-skórne z dodatnim wynikiem EBV
ang. EBV+ mucocutaneous ulcer, EBVMCU
EBVMCU dotyczy najczęściej osób w wieku bardzo dojrzałym lub chorych, u których stosowano wcześniej leczenie obniżające odporność (metotreksat, azatiopryna, cyklosporyna, anty-TNF i in.)
Objawia się pojedynczymi, ostro odgraniczonymi owrzodzeniami na skórze, błonie śluzowej jamy ustnej i gardła lub przewodu pokarmowego. Przebieg kliniczny jest powolny i zwykle ogranicza się do skóry lub błony śluzowej.
O rozpoznaniu decyduje wynik badania histopatologicznego. Warto wykonać badania obrazowe (TK, PET-TK) i skontaktować pacjenta z immunologiem klinicznym celem oceny pod kątem zaburzeń odporności.
Wewnątrznaczyniowy chłoniak z dużych komórek B
ang. intravascular large B-cell lymphoma, IVL, IVBCL
Charakteryzuje się naciekiem naczyń krwionośnych przez duże, nowotworowe komórki B. Opisano postać pierwotnie skórną, która w chwili rozpoznania występuje tylko w skórze, ale najczęściej choroba zajmuje równocześnie ośrodkowy układ nerwowy, płuca oraz skórę i ma agresywny przebieg.
Zmiany skórne to fioletowawe plamy i tarczki, guzy lub zmiany teleangiektatyczne (z siateczką naczyń) zlokalizowane najczęściej na kończynach dolnych lub tułowiu. O rozpoznaniu decyduje wynik badania histopatologicznego skóry/węzła chłonnego. Konieczne jest wykonanie badań obrazowych TK lub PET-TK. W leczeniu stosuje się polichemioterapię prowadzoną przez hemato-loga.
ZMIANY SKÓRNE - JAK DBAĆ O RANY?
Zmiany na skórze w przebiegu chłoniaków skórnych różnią się w zależności od danego podtypu. Niektóre z nich - wraz z progresją choroby - mogą przyjąć postać ran lub guzów z owrzodzeniami
i goić się przez wiele tygodni czy miesięcy, dlatego ważne jest poznanie metod ich prawidłowej i bezpiecznej pielęgnacji. Pozwoli to zredukować nieprzyjemne objawy związane z ranami oraz zmniejszy ryzyko rozwoju infekcji. Każdy pacjent powinien mieć indywidualnie dobrany i zaplanowany przez lekarza
prowadzącego sposób opieki.
Wszystkie zmiany na skórze, które pojawiają się w przebiegu chłoniaków skóry, wymagają odpowiednio dobranej pielęgnacji. Jednak w sposób szczególny wymagają tego guzy z owrzodzeniami, dlatego właśnie im po-święcimy ten rozdział.
Grudki, guzki czy guzy są wynikiem naciekania skóry przez komórki nowotworowe, co skutkuje utratą jej prawidłowego unaczynienia, a to może pro-wadzić do powstania owrzodzeń. Takim zmianom może towarzyszyć nie-przyjemny zapach, wysięk, krwawienie czy dolegliwości bólowe, a objawy te wpływają na znaczne obniżenie jakości życia pacjentów. Prawidłowa pielęgnacja pomaga łagodzić jednak te dolegliwości.

Należy pamiętać, że trudno gojące się rany wynikające z chłoniaka skóry są jedynie jego objawem. Kluczowe jest leczenie choroby podstawowej, a samo zaopatrzenie i pielęgnacja ran stanowi wsparcie terapii - niemniej jednak jest bardzo ważną i integralną częścią leczenia.
ZMIANA OPATRUNKU I PIELĘGNACJA RANY
Monoterapia z rytuksymabem, którą czasem pro-ponuje się pacjentom z małą masą guza, to zwy-kle 4 dawki podawane w odstępie tygodnia, z na-stępowym leczeniem podtrzymującym (dawki le-ku co 2-3 miesiące w kolejnych 2 latach).
Zmianę opatrunku rozpoczynamy od przygotowania odpowiedniego stanowiska, o sterylność którego dbamy na miarę domowych warunków. Ważne, żeby upewnić się przed przystąpieniem do pielęgnacji rany, że mamy wszystkie potrzebne materiały.
Podstawowy zestaw powinien zawierać:
- płyn do dezynfekcji rąk
- rękawiczki jednorazowe
- płyny do oczyszczania rany (sól fizjologiczna, lawaseptyk)
- metalowe nożyczki do przycinania opatrunków (przeznaczone tylko do tego celu, czyste i zdezynfekowane)
- opatrunki specjalistyczne
- podkład higieniczny
- włókninowy przylepiec do podtrzymania opatrunku lub bandaż
- pozostałe środki zalecone przez lekarza mające zastosowanie w leczeniu ran
- pojemnik lub worek na odpady medyczne
Przed przygotowaniem stanowiska do zmiany opatrunku zawsze należy umyć ręce.
Po przygotowaniu stanowiska przechodzimy do zdjęcia poprzedniego opatrunku oraz wstępnego oczyszczenia skóry wokół rany, co robimy w czterech etapach.
1.Zdezynfekuj ręce i nałóż jednorazowe rękawiczki
2.Pielęgnację rany rozpoczynamy od zdjęcia poprzedniego opatrunku. W razie jego przyschnięcia do rany należy obficie polać go solą fizjologiczną i powoli zdejmować.
3.Następnym krokiem jest dokładne umycie skóry WOKÓŁ rany z pomocą dedykowanych środków myjących oraz gazików. Pamiętaj, aby myjąc skórę wokół rany, omijać samą ranę, którą oczyścisz w kolejnym kroku.
4.Następnie przechodzisz do wstępnego oczyszczenia rany z użyciem gazików oraz lawaseptyku, który pozwala na usunięcie zanieczyszczeń, wysięku i krwi,a także dodatkowo zapewnia nawilżenie rany.
5.Stary opatrunek oraz brudne rękawiczki należy wyrzucić do worka na odpady medyczne, a ręce zdezynfekować.
Kiedy już rana jest wstępnie przygotowana, przechodzimy do właściwej pielęgnacji. Podstawą procesu terapeutycznego trudno gojących się ran jest właściwe opracowanie rany i leczenie miejscowe w oparciu o strategię określaną akronimem TIMERS.
- Tissue debridement – oczyszczenie rany.
- Infection and inflammation control – kontrola infekcji i stanu zapalnego.
- Moisture balance – utrzymanie odpowiedniego poziomu wilgoci w ranie.
- Edges, epidermization stimulation – ochrona brzegów rany oraz stymulacja naskórkowania.
- Regeneration/repair of tissue – regeneracja i naprawa tkanek.
- Social and individual-related factors – działania mające na celu edukację pacjenta i jego rodziny, zaangażowanie go w proces leczniczy oraz zadbanie o jego zdrowie psychiczne.
T OCZYSZCZENIE RANY
1.Załóż nowe rękawiczki
2.Delikatnie usuń mocniej przylegające zanieczyszczenia oraz włóknik, czyli luźne tkanki w ranie – z pomocą dedykowanych jałowych gąbek / ściereczek / opatrunków. Jeśli guz przy najmniejszym kontakcie z gazą krwawi, a czyszczenie sprawia pacjentowi ból, należy odstąpić od tego kroku.
3.Zdejmij rękawiczki, zdezynfekuj dłonie i załóż nowe rękawiczki.
I KONTROLA INFEKCJI I PROCESU ZAPALNEGO
Rany nowotworowe cechuje przewlekły stan zapalny, obecność drobnoustrojów w formie biofilmu oraz brak tendencji do samoistnego gojenia. Sama kolonizacja rany przez drobnoustroje nie jest równoznaczna z infekcją, może jednak do niej prowadzić, a ponieważ infekcje stanowią dodatkowy czynnik zakłócający i wydłużający proces gojenia, dlatego tak ważne jest, aby nie dopuścić do rozwoju infekcji.
Sprawdź, czy nie pojawiły się lub nasiliły objawy infekcji miejscowej lub uogólnionej. Jeśli tak – skontaktuj się z lekarzem.
OBJAWY INFEKCJI MIEJSCOWEJ
- zaczerwienienie
- obrzęk
- ocieplenie skóry wokół rany
- zwiększony lub ropny wysięk
- ból
OBJAWY INFEKCJI UOGÓLNIONEJ
- gorączka
- apatia
- utrata apetytu
- złe samopoczucie, osłabienie ogólne pogorszenie
stanu chorego
Zgodnie ze strategią racjonalnego zarządzania środkami przeciwdrobnoustrojowymi wskazane jest unikanie niepotrzebnego i nieuzasadnionego stosowania antyseptyków oraz terapii o zbyt szerokim spektrum działania,
w tym stosowania antybiotyków.
Należy podkreślić, że w przypadku zakażenia miejscowego rana powinna być leczona przede wszystkim antyseptycznie, czyli dbając o jej regularne odkażanie – nie stosujemy antybiotyków miejscowych! W przypadku wystąpienia infekcji uogólnionej lub nasilenia objawów infekcji miejscowej lekarz może zalecić antybiotykoterapię ogólną.
Postępowanie powinno być indywidualnie dopasowane do konkretnej sytuacji chorego.
M odpowiedni poziom wilgoci w ranie
Jednym z czynników wpływającym na prawidłowe gojenie rany jest utrzymanie w niej odpowiedniej wilgoci. Z jednej strony musimy zadbać, aby nie było w niej zbyt dużego wysięku, co może prowadzić do niepożądanej maceracji skóry, z drugiej nie powinna być zbyt sucha, co nie sprzyja proce-sowi gojenia. W zachowaniu odpowiedniego poziomu wilgoci w ranie pomagają nam właściwie dobrane opatrunki.
RODZAJE OPATRUNKÓW SPECJALISTYCZNYCH
Rany w przebiegu chłoniaków skórnych mogą być bardzo zróżnicowane, np. z przewagą wysięku lub przewagą tkanki obumarłej. Na szczęście nowoczesne opatrunki odpowiadają na wiele różnych potrzeb. W zależności od rodzaju tych tkanek w ranie, obecnych objawów infekcji czy ilości wysięku, zostanie dobrany odpowiedni. Należy wybrać taki, który zapobiegnie zanieczyszczeniu i zminimalizuje ryzyko infekcji. Odpowiedni opatrunek powinien zapewniać wilgotne środowisko w ranie, skutecznie odprowadzając wysięk oraz zapobiegając namnażaniu się bakterii czy maceracji skóry wokół rany.
Jeśli rana ma tendencję do krwawienia, można zastosować opatrunki alginianowe, które mają właściwości hemostatyczne lub opatrunki nieprzywierające.
Owrzodzenia z centralną martwicą można zabezpieczyć nieprzywierającym opatrunkiem siatkowym, a dopiero następnie należy nałożyć opatrunek wierzchni – takie działanie ma na celu redukcję ryzyka przywarcia opatrunku do rany i jej uszkodzenia podczas kolejnej zmiany opatrunku.
Na rany z dużym wysiękiem należy zastosować opatrunki chłonne (piankowe, superabsorbenty).
Na rany z nasilonym nieprzyjemnym zapachem można zastosować opatrunki z węglem aktywowanym lub substancjami antybakteryjnymi.
Właściwe opatrunki pomoże Ci dobrać Twój lekarz lub pielęgniarka w ośrodku prowadzącym Twoje leczenie.
Zanim założysz opatrunek, zapoznaj się z kolejnym krokiem, jakim jest ochrona skóry wokół rany.
E OCHRONA BRZEGÓW RANY i STYMULACJA NASKÓRKOWANIA
Należy pamiętać o pielęgnacji skóry wokół rany, aby zmniejszyć ryzyko uszkodzenia skóry przez opatrunki oraz o zabezpieczaniu brzegów rany stosując maści o właściwościach hydrofobowych np. wazelinę.
Kiedy już oczyścisz i opracujesz ranę oraz sprawdzisz objawy infekcji, przed założeniem odpowiedniego opatrunku, pamiętaj, aby zabezpieczyć brzegi rany oraz zdrową skórę wokół niej.
1.Jeśli maść nakładasz ręką, ponownie zmień rękawiczki. Jeśli chcesz uniknąć zmiany rękawiczek, maść nałóż szpatułką.
2.Po zabezpieczeniu brzegów rany, czas założyć opatrunek, który można umocować włókninowym przylepcem bezpośrednio do skóry lub delikatnym bandażem.
R REGENERACJA I NAPRAWA TKANEK
W akronimie TIMERS literka R oznacza szeroko pojęte działania zmierzające do regeneracji tkanek. Dotyczy to różnych metod i procedur, które może zalecić lekarz w celu wsparcia procesu regeneracji tkanek oraz wykluczenia czynników, które mogą mieć wpływ na opóźnienie gojenia ran.
S EDUKACJA PACJENTA ORAZ ZDROWIE PSYCHICZNE
Pielęgnacja ran może przynieść ulgę fizyczną i jest bardzo ważnym elementem leczenia choroby, natomiast w doborze protokołu pielęgnacyjnego bierzemy także pod uwagę czynniki społeczne oraz indywidualne, które mogą wpływać na samopoczucie pacjenta.
Dlatego zawsze – jeśli pacjent potrzebuje – należy wskazać możliwości wsparcia emocjonalnego. W tym poradniku kolejny rozdział jest właśnie o tym, jak radzić sobie psychicznie z faktem pojawienia się w życiu choroby, która powoduje powstawanie na skórze zmian i tych mniejszych, i tych trudno gojących. Zapraszamy Cię do lektury!
Jest to oczywiście bardzo indywidualne, ale zazwyczaj zmiany opatrunków specjalistycznych dokonujemy mniej więcej co 3-5 dni lub wcześniej, jeśli opatrunek przesiąknie. Raz założony opatrunek może zabezpieczać Twoją ranę nawet do kilku dni, dlatego tak ważny jest jego właściwy dobór.
Odpowiednia pielęgnacja rany i dobrze dobrane opatrunki zmniejszają ryzyko rozwoju infekcji i powikłań związanych z ranami, a także mają przełożenie na poprawę jakości życia pacjentów z chłoniakami skóry.
Jak widzisz, zmiana opatrunków to proces dość złożony, ale postępując zgodnie z zaleceniami, każda kolejna zmiana może stać się łatwiejsza. Opatrunki może zmieniać pacjent lub opiekun.
Jeśli potrzebujesz profesjonalnego wsparcia skontaktuj się ze swoim lekarzem POZ i poproś o pomoc pielęgniarki środowiskowej.
Odbicie w lustrze czyli jak radzić sobie ze zmianami w wyglądzie?
„I zawsze pamiętaj, że jesteś kimś wyjątkowym. Jedyne, co musisz zrobić, to pozwolić innym zobaczyć, że taka/taki jesteś.”
Milton H. Erickson, psychoterapeuta
Chłoniak skóry to więcej niż zwykły nowotwór. Wyzwaniem jest nie tylko sama choroba i leczenie. Wyzwaniem jest codzienne funkcjonowanie ze zmianami skórnymi.
Patrzysz w lustro albo po prostu na swoje ciało i doświadczasz wielu przykrych, trudnych uczuć i myśli na swój temat. I to jest absolutnie normalne
i naturalne. Nasze ciało, nasz wygląd jest ważną częścią nas… na szczęście NIE jedyną i NIE najważniejszą. Jeśli uważasz, że jedyną i najważniejszą, tym bardziej zapraszam Cię do przeczytania tego, co chcę Ci przekazać.
Przeczytaj proszę uważnie zaznaczone w tekście pogrubioną czcionką pytania i pozwól sobie na podążanie za tym, co przynoszą Twoje i moje odpowiedzi.
Akceptacja choroby nie oznacza poddania się, ale uznanie jej obecności
i skoncentrowanie się na możliwościach radzenia sobie z nią. Praktyka ak-ceptacji może pomóc w zmniejszeniu stresu i lęku związanego z wyglądem.
Wygląd jest ważną częścią Twojej tożsamości. Wpływa na sposób, w jaki postrzegasz siebie. Dlatego ma swój udział w poczuciu własnej wartości. Poczucie własnej wartości zaś osadza Cię w świecie innych ludzi i oddziałuje na Twój stan psychiczny i samopoczucie.
Zmiany skórne w chłoniaku skóry są trudne do zaakceptowania, zwłaszcza gdy są umiejscowione na odsłoniętych częściach ciała, takich jak twarz, szyja
Akceptacja choroby nie oznacza poddania się, ale uznanie jej obecności i skoncentrowanie się na możliwościach radzenia sobie z nią. Praktyka akceptacji może pomóc w zmniejszeniu stresu i lęku związanego z wyglądem.
Wygląd jest ważną częścią Twojej tożsamości. Wpływa na sposób, w jaki postrzegasz siebie. Dlatego ma swój udział w poczuciu własnej wartości. Poczucie własnej wartości zaś osadza Cię w świecie innych ludzi i oddziałuje na Twój stan psychiczny i samopoczucie.
Zmiany skórne w chłoniaku skóry są trudne do zaakceptowania, zwłaszcza gdy są umiejscowione na odsłoniętych częściach ciała, takich jak twarz, szyja, czy ręce. Codziennym wyzwaniem staje się własne odbicie w lustrze. Jeśli nie patrzysz się na siebie, to prawdopodobnie dlatego, bo nie chcesz się taką/takim widzieć. „Nie chcę taka/taki być”. To właśnie przekazujesz sobie i całemu światu. Ale czy to coś zmieni? Nie, to tylko jeszcze bardziej pogorszy Twoje samopoczucie. Jeśli Twoje nastawienie to opór wobec tego, co jest rzeczywistością, to jakie uczucia pojawiają się w Tobie? Rozżalenie, złość, bezradność, przygnębienie. Twój stan psychiczny zamiast się poprawiać, będzie się pogarszał, bo ciągle będziesz w oporze wobec tego, co jest faktem – masz zmiany na skórze. Co z tym możesz zrobić? Zauważ, że pomijam w tym momencie cały obszar wiedzy dermatologicznej i pielęgnacyjnej. Skupiam się na tym, co oprócz konsultacji ze specjalistami od skóry możesz zrobić dla siebie. Skoryguj sposób, w jaki myślisz o sobie, kiedy widzisz zmiany skórne.
Sprawdź najpierw, w jaki sposób myślisz teraz?
„to okropne, jak wyglądam!”
„kiedyś to byłam/byłem ja…
ale teraz już nie jestem sobą …”
„nie mogę na siebie patrzeć!”
„jeśli tak będę wyglądać dalej… to nie chcę…”
TE MYŚLI CI SZKODZĄ. SĄ BLOKADĄ W ZDROWIENIU
Czy możesz myśleć inaczej?
TAK. Masz wpływ na swoje myśli, bo to tylko myśli w Twojej głowie, najczęściej tworzą się bez udziału Twojej świadomości, czyli automatycznie. Tak działa Twój i mój umysł. Zapisz na kartce papieru myśli, które są w Twojej głowie na temat Twojego wyglądu. A potem zadaj sobie pytanie: jak inaczej chcę o tym myśleć… i obok zapisz jedną albo więcej myśli.
PODPOWIEM CI KILKA
„Choroba jest częścią mojego życia, wygląd jest częścią mojego życia, ale nie definiuje tego, kim jestem.”
„Chłoniak skóry to moje wyzwanie. Wierzę, że moja wartość jako człowieka nie ma związku z wyglądem.”
„Jestem kimś więcej niż mój wygląd.”
„Mam cele i marzenia, do których dążę, niezależnie od mojej choroby i wyglądu.”
„Każdy krok, który podejmuję, przybliża mnie do lepszego samopoczucia i realizacji moich celów.”
„Myśli to tylko myśli. Mogę je zmieniać… i przestać w nie wierzyć, że są rzeczywistością.”
„Patrzę na swoje życie w szerszej perspektywie i nie pozwalam, aby choroba i związany z nią wygląd dominowały nad wszystkim.”
Uświadom sobie, że negatywne myśli są tylko myślami, niekoniecznie rzeczywistością. Nie musisz wierzyć w każde negatywne przekonanie, które pojawia się w Twojej głowie.
Jeśli uruchomisz swoją kreatywność, to znajdziesz jeszcze kilka, a może więcej takich myśli o sobie i swoim aktualnym wyglądzie, dzięki którym łatwiej Ci będzie radzić sobie z trudnymi emocjami i łatwiej Ci będzie wzmacniać swoją pewność siebie.
Jeśli masz napisane myśli, które chcesz myśleć, to pozostaje teraz wprowadzić je do mózgu, aby przejęły kontrolę nad sposobem myślenia o swoim wyglądzie. W tym celu możesz:
- Napisać je na kartkach, karteczkach, aby były w każdym miejscu domu i „rzucały się w oczy”.
- Nagrać na dyktafonie w telefonie te myśli i odsłuchiwać je tak często, jak to jest możliwe.
- Wykonywać codziennie wizualizację (najlepiej poprzedzoną relaksacją), w której wyobrażasz sobie, jak te myśli wpływają do Twojej głowy i tam stają się silniejsze od tych, które Ci nie służą.
Pamiętaj, że zmiana myślenia to proces, który wymaga czasu i cierpliwości. EFEKTY DAJE ILOŚĆ POWTÓRZEŃ. Warto zainwestować czas, energię i wysiłek, bo te myśli będą dodawać Ci wiary w siebie. Będą też wspierać AKCEPTACJĘ, czyli uznanie rzeczywistości taką, jaka jest.
Akceptacja jest pierwszym krokiem w radzeniu sobie z trudną sytuacją, jaką przyniosło nam życie. Jest potrzebna, bo dopiero, kiedy coś zaakceptujemy, mamy szansę skupić się na poszukaniu rozwiązań, pomysłów i aktywności w sytuacji, która jest dla nas trudna i nie mamy nad nią kontroli. Ale nawet, jeśli nie mamy nad sytuacją kontroli, to wciąż mamy wpływ na nasze nastawienie do niej. I właśnie to jest sposób radzenia sobie z tym, co przynosi nam życie: skupianie się na tym, na co możemy wpływać. Jeśli nauczysz się wpływać na swoje myśli: obserwować je, zmieniać i modyfikować, to będzie Ci łatwiej w kontakcie ze światem zewnętrznym.
Oprócz swojego nastawienia, czyli myśli, na co masz jeszcze wpływ?
Wspomniałam o tym wcześniej, ale przypomnę dla wzmocnienia przekazu. Kosmetologia i środki dermatologiczne w obecnych czasach stwarzają szereg możliwości zarówno pielęgnacyjnych, jak również kamuflujących zmiany skórne. Nawet drobne „poprawki” wpłyną na samoocenę i samopoczucie.
Czy znasz techniki „kamuflażu”?
Konsultacja z ekspertem, który doradzi w jaki sposób tuszować widoczne zmiany skórne, a potem stosowanie technik kamuflażu w codziennym funkcjonowaniu jest ważną częścią wspierania siebie i ulepszania jakości życia w chorobie.
Widoczne zmiany skórne mogą powodować uczucie wyobcowania i lęk przed negatywnymi reakcjami innych ludzi. Jeśli często obawiasz się stygmatyzacji i odrzucenia społecznego, to prawdopodobnie unikasz kontaktów społecznych, a może nawet się izolujesz.
WYGLĄD JEST CZĘŚCIĄ TWOJEJ TOŻSAMOŚCI, ALE NIE DEFINIUJE CIĘ JAKO CAŁOŚCI, JAKO CZŁOWIEKA, JAKO OSOBY, JAKO KOBIETY CZY MĘŻCZYZNY.
Jak myślisz, co naprawdę się liczy w interakcjach ludzkich? Czy ludzi, których znasz, pamiętasz dlatego, że tak wyglądają, czy dlatego, że jacyś są?
Ludzie pamiętają, jak ich traktujemy, NIE jak wyglądamy. Przypomnij sobie, co jest najważniejsze w relacjach z innymi i przenieś swoją uwagę z wyglądu na to, co naprawdę się liczy.
A co naprawdę się liczy?
Zrób listę Twoich cech, umiejętności, zasobów wewnętrznych, na przykład wiedzy czy doświadczeń, za które inne osoby Cię cenią, szanują, lubią.
Jak myślisz, za co Cię cenią i szanują Inni?
Co lubią w Tobie inni?
Czym inspirujesz innych?
Jest prawie pewne, że jeśli sama/sam siebie nie lubisz i nie cenisz, to będziesz miała/miał kłopoty z odpowiedzią na powyższe pytania. Dlatego odpowiedz teraz na te same pytania, ale tak jakbyś pytała/pytał siebie samą/samego.
Za co się cenisz i szanujesz?
Co w sobie lubisz?
W jakim stopniu kochasz tę część siebie, która NIE JEST ciałem i wyglądem?
W jakim stopniu kochasz tę część siebie, która JEST ciałem i wyglądem?
Odpowiedzi na te wszystkie pytania pozwolą Ci zrozumieć, że barierą nie jest Twoja choroba i wygląd z nią związany, ale to jak myślisz o sobie.
To, jak myślisz o sobie, kiedy jesteś sama/sam NIE ZNIKA, kiedy wychodzisz do świata zewnętrznego. Staje się filtrem (to tak, jak okulary), przez który patrzysz. Jeśli twoim filtrem jest obawa: „odstraszam swoim wyglądem”, to wyraz twarzy Twojego znajomego odbierasz jako oznakę politowania, a nie serdeczności i wsparcia. Jeśli zmienisz filtr (Twój sposób myślenia o swoim wyglądzie), zmienisz także odbiór tego, co przekazują Ci ludzie w kontakcie z Tobą. Uświadom sobie, że praktycznie dopóki ktoś nam nie powie, co myśli, to zawsze jest to tylko nasze wyobrażenie tego, co ma w głowie na nasz temat. Ale czy nasze wyobrażenie jest zgodne z rzeczywistością mentalną naszego rozmówcy? Najczęściej nie. Powiedziałabym nawet, że prawie zawsze jest NIEZGODNE. Dlatego nie wyobrażaj sobie i nie zakładaj, co myślą na temat Twojego wyglądu inni ludzie. Filtr: „wyglądam jak wyglądam, ale ważniejsze jest być teraz z nim/nią/nimi” pozwoli Ci odczytywać przekazy innych ludzi (ich słowa, zachowania werbalne i niewerbalne) bez odniesienia do Twojego wyglądu. Okaże się wtedy, że ZMIANY SKÓRNE NIE ZMIENIŁY CIEBIE i waż-na/ważny jesteś Ty z całym swoim wewnętrznym światem.
Każde wyjście do ludzi, nawet jeśli jest trudne, jest krokiem w stronę budowania pewności siebie. Dlatego dołącz do swoich codziennych przypominajek zdrowych myśli to zdanie:
„Każdy krok na zewnątrz, do ludzi, jest krokiem do przodu.”
AUTORZY PORADNIKA
Małgorzata Sokołowska-Wojdyło
Wojciech Jurczak
Hanna Tchórzewska-Korba
Magdalena Antoszewska
Beata Pachońska
Pełną treść poradnika znajdziesz tutaj:



