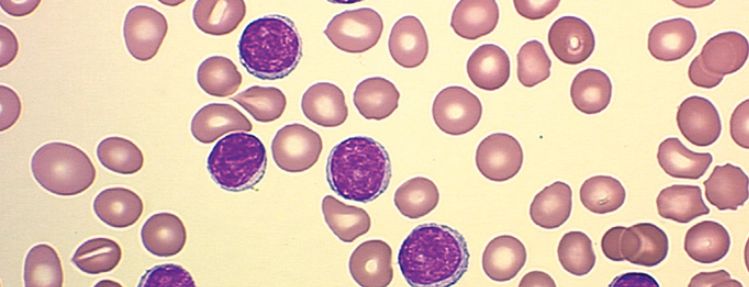
PRZEWLEKŁA BIAŁACZKA LIMFOCYTOWA
- ang. Chronic Lymphocytic Leukemia
- międzynarodowy skrót: CLL
Przewlekła białaczka limfocytowa – PBL – należy do grupy nowotworów układu chłonnego zwanych chłoniakami. Jest chorobą nowotworową, w której z niewyjaśnionych przyczyn dochodzi do zwiększenia tempa wytwarzania nieprawidłowych limfocytów B i wydłużenia czasu ich przeżycia.
- PRZEWLEKŁA BIAŁACZKA LIMFOCYTOWA - co to znaczy?
- JAKIE OBJAWY TOWARZYSZĄ PBL - skąd wiem, że choroba się rozwija?
- DIAGNOSTYKA PBL - czyli jakie badania zleci Ci lekarz?
- JAK WYGLĄDA STRATEGIA WATCH & WAIT - przed leczeniem oraz w trakcie remisji?
- KIEDY ZAPADA DECYZJA O PODJĘCIU LECZENIA - za pierwszym razem, jak i we wznowie choroby?
- LECZENIE PRZEWLEKŁEJ BIAŁACZKI LIMFOCYTOWEJ
- PROGRAM LEKOWY
- WYBRANE DZIAŁANIA NIEPOŻĄDANE obserwowane podczas lub/i po leczeniu
- WAŻNE kiedy skontaktować się z lekarzem!
- SYTUACJE SZCZEGÓLNE
PRZEWLEKŁA BIAŁACZKA LIMFOCYTOWA co to znaczy?
DLACZEGO PBL NAZYWAMY CHOROBĄ PRZEWLEKŁĄ?
Układ chłonny składa się z węzłów chłonnych, śledziony i skupisk tkanki limfatycznej w części narządów wewnętrznych. Wytworzone tam limfocyty krążą we krwi. W przewlekłej białaczce limfocytowej układ chłonny zaczyna produkować nadmiar nieprawidłowych limfocytów – wyglądem i wielkością bardzo przypominających prawidłowe komórki, które często mają dodatkowo upośledzony pro-ces zaprogramowanej śmierci (tzw. apoptozy). Sprawia to, że ich liczba we krwi i szpiku jest zbyt duża. Takie limfocyty nazywamy potocznie białaczkowymi, a ich nadmierna akumulacja może prowadzić do wypierania innych, nie-zbędnych do życia, linii komórkowych (np. krwinek czerwonych, płytek krwi), a także powiększenia węzłów chłonnych czy śledziony.
Bardziej obrazowo można powiedzieć, że nowe komórki ciągle powstają, a że wszystkie żyją dłużej, jest ich coraz więcej – w konsekwencji – stanowczo za dużo. Wyobraź sobie, jak wzrosłaby liczba ludzi na ziemi, gdyby ilość urodzin zwiększyła się, a średnia długość życia wydłużyła do 300 lat.
Ten proces, choć niepożądany, jest jednak najczęściej i przez większość czasu dość powolny, dlatego pomimo pojawienia się w organizmie choroby, przebiega ona w sposób łagodny, skryty, a objawy kliniczne u chorych mogą być bardzo dyskretne lub nie występować w ogóle.
Z tego też powodu pierwsze podejrzenie PBL pojawia się najczęściej „przypadkiem”, np. analizując badanie morfologii zlecone z innych przyczyn. Wówczas konieczna jest konsultacja hematologa, zlecenie dodatkowych badań i potwierdzenie wstępnego rozpoznania. Samo potwierdzenie rozpoznania PBL i obecności podwyższonej (nawet znacząco) liczby limfocytów we krwi obwodowej nie stanowi wskazania do rozpoczęcia leczenia.
WATCH & WAIT Obserwuj i czekaj.
Często, po przypadkowym rozpoznaniu choroby, najwłaściwszym podejściem jest obserwacja chorego, czyli tzw. strategia watch and wait. W tym czasie odbywają się kontrolne wizyty oraz badania, a terapię rozważa się, gdy produkcja komórek nieprawidłowych przyspiesza, pacjent zaczyna odczuwać objawy, a wyniki badań krwi pogarszają się. Wówczas leczymy chorobę, doprowadzając do jej cofnięcia się – remisji – choć nie całkowitego wyleczenia i powracamy do jej obserwacji.
ROKOWANIE
W większości przypadków, pomimo obecności nowotworu w organizmie, można żyć z tą chorobą przez wiele lat, prowadząc normalne życie, lecząc ją okresowo „raz na jakiś czas”, często – nie od razu po rozpoznaniu. Coraz większa liczba pacjentów chorych na PBL umiera z przyczyn naturalnych, nie związanych z tą chorobą nowotworową.
SKĄD WZIĘŁA SIĘ CHOROBA?
Przyczyny przewlekłej białaczki limfocytowej nie są znane, rzadko obserwuje się tendencję do występowania choroby rodzinnie, co może świadczyć o pewnych predyspozycjach genetycznych do wystąpienia tej choroby. Nie ma jednak konieczności wykonywania profilaktycznych badań u dzieci lub rodzeństwa chorych, ani – jeśli choroba dotyczy osób w wieku reprodukcyjnym – rezygnacji z chęci posiadania potomstwa.
Jednak w trakcie leczenia należy stosować antykoncepcję, gdyż przynajmniej część ze stosowanych leków może uszkadzać plemniki, komórki jajowe czy płód.
EPIDEMIOLOGIA
Przewlekła białaczka limfocytowa jest najczęstszym chłoniakiem u osób dorosłych, rozpoznawanym w szczególności u osób starszych.
- Pacjenci w wieku powyżej 65 r.ż. stanowią ponad 70% chorych na PBL
- Zaledwie 10-15% chorych na PBL ma mniej niż 50 lat
- Mężczyźni chorują prawie 2-krotnie częściej niż kobiety
JAKIE OBJAWY
TOWARZYSZĄ PBL
skąd wiem, że choroba się rozwija?
Początek choroby jest zwykle bezobjawowy, stwierdza się jedynie nieprawidłowości w morfologii krwi pod postacią LEUKOCYTOZY -nadmierna ilość białych krwinek – z LIMFOCYTOZĄ – nadmierna ilość limfocytów. Z czasem, a u części chorych już przy rozpoznaniu, można stwierdzić więcej objawów świadczących o rozwoju choroby i poddających pod rozwagę włączenie leczenia, celem cofnięcia choroby.
LIMFADENOPATIA czyli powiększenie węzłów chłonnych.
Mogą być powiększone zarówno węzły chłonne obwodowe, wyczuwalne w badaniu fizykalnym (np. szyjne, pachowe, nadobojczykowe, pachwinowe), jak i węzły chłonne znajdujące się w śródpiersiu czy wewnątrz jamy brzusznej, widoczne tylko w wykonanych badaniach obrazowych.
SPLENOMEGALIA czyli powiększenie śledziony, również wynikające z nacieku komórek nowotworowych.
Samo powiększenie śledziony, nawet znaczne, jest niebolesne. Stosunkowo często chorzy odczuwają uczucie pełności, zwłaszcza przy posiłkach, czasem wręcz uniemożliwiające zjedzenie całego obiadu. Pojawienie się silnych dolegliwości bólowych pod lewym łukiem żebrowym może być objawem pęknięcia śledziony i wymaga pilnej konsultacji chirurgicznej, zwykle połączonej przynajmniej z badaniem ultrasonograficznym.
NAWRACAJĄCE ZAKAŻENIA
Limfocyty białaczkowe nie produkują białek odpornościowych i jednocześnie ograniczają produkcję limfocytów prawidłowych. Niezależnie od tego, na jakim etapie choroby pojawi się infekcja, u chorego na PBL zawsze należy traktować ją poważnie, liczyć się z jej cięższym przebiegiem, a w skrajnych przypadkach wręcz z za-grożeniem życia. Przed rozpoczęciem leczenia infekcji obowiązkowe jest badanie morfologii, a przy znaczącym spadku liczby granulocytów podawanie czynników wzrostu czy nawet rozważenie hospitalizacji.
Dlatego ZAWSZE, w razie pojawienia się objawów infekcji, skontaktuj się z lekarzem i nie lecz jej na „własną rękę”. Co ważne, jeśli jesteś już w trakcie terapii PBL, w większości przypadków należy okresowo przerwać stosowane leczenie, stąd powinien o tym być poinformowany lekarz prowadzący, aby ustalić właściwe postępowanie.
NIEDOKRWISTOŚĆ (ANEMIA) odczuwana jako osłabienie, senność czy nietolerancja wysiłków.
W sytuacjach, gdy ma ona mechanizm autoimmunologiczny (niszczenia erytrocytów przez własny układ immunologiczny) i jest związana z hemolizą, objawy mogą być bardziej nasilone, towarzyszyć im może żółtaczka (najwcześniej zauważalne jest zażółcenie białkówek oczu).
MAŁOPŁYTKOWOŚĆ (TROMBOCYTOPENIA) i związaną z nią skaza krwotoczna.
Skaza krwotoczna objawia się w postaci małych, czerwonych wybroczyn na błonach śluzowych np. jamy ustnej, skórze kończyn czy tułowia. Pacjenci mogą zauważyć krwawienia z dziąseł, szczególnie podczas mycia zębów, pojawianie się siniaków oraz krwawień bez znanej przyczyny, u kobiet również przedłużające się, obfite krwawienia miesięczne. Skaza krwotoczna może wynikać z nacieku nowotworowych limfocytów B na szpik kostny, co upośledza produkcję płytek krwi (trombocytów). Drugim mechanizmem małopłytkowości może być niszczenie megakariocytów, czyli komórek z których powstają płytki krwi, przez własny układ immunologiczny.
OBJAWY OGÓLNE
Rzadziej obserwuje się charakterystyczne dla chłoniaków OBJAWY OGÓLNE w znaczeniu hematoonkologicznym, tzn.:
- GORĄCZKĘ utrzymującą się ponad 2 tygodnie bez uchwytnej przyczyny.
- NOCNE POTY przeważnie zlewne, wymagające zmiany bielizny nocnej.
- UTRATĘ MASY CIAŁA (utrata ≥ 10% wyjściowej masy ciała w ciągu 6 miesięcy).
DIAGNOSTYKA PBL
czyli jakie badania zleci Ci lekarz?
Jak już wiesz, PBL należy do grupy nowotworów zwanych chłoniakami, a ponieważ jest kilka rodzajów chłoniaków o podobnym obrazie klinicznym, stąd tak niezmiernie ważne jest, aby wykonać odpowiednie badania, które pozwolą na dokładne ustalenie, czy na pewno chorujesz na PBL. Od momentu podejrzenia tej choroby do postawienia ostatecznego rozpoznania mogą upłynąć nawet 2 miesiące. W ramach diagnostyki należy jednak nie tylko potwierdzić obecność samej choroby, ale także ocenić stadium jej klinicznego zaawansowania. W sytuacjach wymagających leczenia niezbędne są dodatkowe badania – pozwalające m.in. na dokładną charakterystykę zaburzeń genetycznych komórek nowotworowych, czy określenie innych czynników ryzyka. To wszystko ma decydujący wpływ na określenie rokowania u pacjenta oraz wybranie optymalnej terapii.
PIERWSZA WIZYTA oraz wizyty kontrolne i obserwacja.
W czasie pierwszej wizyty lekarz przeprowadzi wywiad, z uwzględnieniem wszystkich chorób przebytych i towarzyszących – warto się do tego przygotować, wziąć historię chorób, zapisać wszystkie zażywane leki oraz suplementy, a także informować w czasie wizyt kontrolnych o zmianach w tym zakresie. Ponadto lekarz oceni wydolność kluczowych narządów (układów).
W czasie diagnostyki, obserwacji i leczenia, w zależności od występowania objawów wymagających monitorowania, zlecane będą odpowiednie badania specjalistyczne.
MORFOLOGIA KRWI OBWODOWEJ
Badanie to może być u chorych na PBL zlecane w pierwszym okresie po postawieniu rozpoznania stosunkowo często (nawet raz w miesiącu), jednak po upewnieniu się, że nie mamy do czynienia z chorobą o większej dynamice, wystarczają później zwykle kontrole co 3-6, a nawet 12 miesięcy.
Musimy jednak pamiętać o konieczności dodatkowych badań w przypadku każdej poważnej infekcji czy pojawienia się objawów skazy krwotocznej. Aby to powiedzieć w sposób jeszcze bardziej jednoznaczny – konieczna jest kontrola morfologii w każdym przypadku, gdy pojawia się gorączka lub inne objawy infekcji, choć możesz wówczas czuć się źle i nie mieć najmniejszej ochoty na dodatkowe badania.
Należy pamiętać, że wynik morfologii pozwoli lekarzowi pierwszego kontaktu zlecić właściwe leczenie infekcji, które – w pojedynczych przypadkach – musi odbywać się w szpitalu, z możliwością podania dożylnych antybiotyków. Od zrozumienia tych zasad zależy Twoje bezpieczeństwo.
BADANIA IMMUNOFENOTYPOWE (CYTOMETRIA PRZEPŁYWOWA)
Badania te mogą zostać wykonane z krwi obwodowej, szpiku kostnego lub aspiratu węzła chłonnego. Przewlekła białaczka limfocytowa jest jednym z wyjątków pośród chłoniaków: do jej rozpoznania nie jest niezbędne badanie histopatologiczne. Może je w większości przypadków zastąpić właśnie badanie immunfenotypowe.
Immunofenotyp jest to indywidualny zestaw białek (antygenów) obecnych na powierzchni komórek. W większości przypadków pozwala rozróżnić komórki białaczkowe od komórek prawidłowych oraz komórki PBL od komórek innych podtypów chłoniaków. Podstawowym kryterium diagnostycznym PBL jest stwierdzenie we krwi obwodowej mono-klonalnych limfocytów B w liczbie co najmniej 5 G/l (czyli 5000 w µl) utrzymujących się powyżej 3 m-cy i cechujących się występowaniem na powierzchni komórki antygenów CD5, CD19, CD20 i CD23 oraz restrykcją łańcuchów lekkich immunoglobulin (obecne są jedynie kappa lub lambda).
POBRANIE WĘZŁA CHŁONNEGO DO BADANIA HIST-PAT
Standardowo w PBL nie wykonuje się pobrania węzła chłonnego, jednak jest to wskazane w przypadku podejrzenia chłoniaka z małych limfocytów lub w przypadku transformacji Richtera, czyli przekształcenia PBL do bardziej agresywnej choroby. Pobranie węzła chłonnego jest krótkim zabiegiem wykonywanym w znieczuleniu miejscowym.
BADANIA SZPIKU
Szpik kostny najczęściej pobiera się z górnego tylnego kolca kości biodrowej. Innym możliwym miejscem pobrania materiału jest mostek. Zabieg ten wykonywany jest w znieczuleniu miejscowym i trwa ok. 5-10 minut. Biopsja szpiku kostnego polega na pobraniu płynnej frakcji szpiku, w której zawarte są komórki. W trepanobiopsji pobierany jest fragment tkanki, co pozwala na badanie pod mikroskopem utkania szpiku kostnego.
W przewlekłej białaczce limfocytowej badania szpiku nie są konieczne do postawienia rozpoznania. Czasami są jednak one pomocne dla różnicowania przyczyny niedokrwistości: czy jej przyczyną są nacieki białaczkowe w szpiku kostnym, czy też procesy autoimmunizacyjne.
POZOSTAŁE BADANIA Z KRWI OBWODOWEJ
Przy podejrzeniu hemolizy zleca się badanie poziomu bilirubiny (bezpośredniej i pośredniej) oraz odczynu Coombsa. Badanie to jest wykonywane z krwi obwodowej i pozwala na ocenę „opłaszczenia” krwinek czerwonych przez przeciwciała (co powoduje ich hemolizę, czyli zniszczenie). U chorych na PBL z niedo-krwistością hemolityczną wynik bezpośredniego testu antyglobulinowego (BTA) – odczynu Coombsa – jest zwykle dodatni.
W przebiegu przewlekłej białaczki limfocytowej stosunkowo często obserwujemy hipogammaglobulinemię – obniżenie stężenia immunoglobulin – która może być przyczyną nawracających infekcji. W części przypadków jest to wskazanie do prowadzenia u chorych substytucji gammaglobulin.
W zależności od wskazań i chorób towarzyszących lekarz może zlecić dodatkową ocenę czynności nerek i wątroby.
BADANIA OBRAZOWE
Do oceny klinicznego zaawansowania nie ma, w większości przypadków, konieczności wykonywania tomografii komputerowej. Przeważnie wykonuje się USG jamy brzusznej oraz RTG klatki piersiowej. Badanie pozytonowej tomo-grafii emisyjnej (PET, z ang. positron emission tomography) nie ma zastosowania u chorych na PBL, z wyjątkiem przypadków transformacji Richtera lub jej podejrzenia.
BADANIA WIRUSOLOGICZNE
Badania wirusologiczne są ważne u chorych na przewlekłą białaczkę limfocytową, ponieważ upośledzenie odporności związane z samą chorobą lub jej leczeniem może prowadzić do częstszych infekcji lub reaktywacji przebytych niegdyś infekcji wirusowych.
Badania wirusologiczne pozwalają na wyszuka- nie w organizmie ludzkim przeciwciał skierowa-nych przeciwko konkretnym wirusom lub materiału genetycznego wirusa.
- Przeciwciała typu IgG świadczą o nabytej odporności (czyli o przebyciu zakażenia lub szczepieniu).
- Przeciwciała typu IgM świadczą o aktywnie toczącym się zakażeniu.
- wirus zapalenia wątroby typu B,
- wirus zapalenia wątroby typu C,
- wirus HIV.
- delecji 11q i 17p metodą fluorescencyjnej hybrydyzacji in situ (FISH, z ang. fluorescent in situ hybridization),
- w razie nieobecności del17p, również mutacji genu TP53 metodami biologii molekularnej;
- konieczne jest również określenie statusu mutacji genów immunoglobulin (IGHV);
- do innych badań genetycznych należy ocena kariotypu – polegająca na wizualnej ocenie chromosomów (struktur komórki z materiałem genetycznym/DNA) celem wykrycia brakujących chromosomów, złamań w ich ramionach czy przemieszczeń fragmentów chromosomów pomiędzy nimi.
- z obecnością chorób współistniejących tzw. UNFIT
- lub bez znacznych obciążeń wynikających z chorób współistniejących tzw. FIT
JAK WYGLĄDA STRATEGIA
WATCH & WAIT
przed leczeniem oraz w trakcie remisji
Pacjenci z rozpoznaną PBL, nie mający jeszcze wskazań do leczenia, powinni być w stałej kontroli, by optymalnie wybrać czas jego rozpoczęcia. Podobnie, chorzy w remisji po zakończeniu kolejnych linii leczenia (wolni od obecności choroby) powinni regularnie zgłaszać się na kontrole lekarskie do prowadzącego specjalisty.
Najczęściej proponuje się chorym:
1. Kontrolę morfologii co 6-12 miesięcy (wcześniej w razie każdej po-ważnej infekcji, pojawienia się skazy krwotocznej czy innych niepokojących objawów). Kontrolę prób nerkowych oraz wątrobowych co 6-12 miesięcy.
2. Badania USG brzucha, miednicy i obwodowych węzłów chłonnych, z podaniem wymiarów węzłów i śledziony co 12 miesięcy (najlepiej, gdy te cykliczne badania wykonuje w kolejnych latach jeden ultrasonografista).
3. Kontrolę u lekarza prowadzącego (hematologa, onkologa lub lekarza pierwszego kontaktu) co 6-12 miesięcy lub wcześniej w razie pojawienia się jakichkolwiek niepokojących objawów. Alternatywą są częstsze konsultacje, których terminy wyznaczane są „na sztywno” co 1-3 miesięcy. Pierwszy plan postępowania zakłada pełną współpracę chorego, jest możliwy jedynie w przypadkach, gdy pacjent zna objawy choroby i możliwe powikłania. Stąd, zanim to się stanie, na początku leczenia/ obserwacji, zwykle proponujemy chorym częstsze wizyty kontrolne.
4. Niezależnie od kontroli PBL nie można zaniedbać leczenia chorób towarzyszących (takich jak cukrzyca czy nadciśnienie) oraz regularnych profilaktycznych badań w celu wczesnej diagnostyki innych chorób nowotworowych, które nieco częściej pojawiają się u chorych na PBL. Jest to także czas na zatroszczenie się o swoją kondycję fizyczną oraz zdrowe odżywianie.
KIEDY ZAPADA DECYZJA O PODJĘCIU LECZENIA
za pierwszym razem, jak i we wznowie choroby
Jak już wcześniej wspomniano, większość chorych w chwili rozpoznania PBL ma stabilną chorobę bez objawów klinicznych i nie wymaga wdrożenia leczenia. Wskazana jest jedynie regularna obserwacja w ramach poradni hematologicznej lub przez lekarza pierwszego kontaktu mającego doświadczenie w obserwacji PBL. Ponieważ jest chorobą przewlekłą, celem terapii nie jest jej wyleczenie, ale kontrola – ograniczenie progresji, poprawa jakości życia oraz jego wydłużenie. Leczenie włącza się zatem, kiedy towarzyszące PBL objawy tego wymagają.
Trzeba pamiętać, że liczba limfocytów może wykazywać znaczne wahania, które nie wynikają z progresji choroby, ale na przykład z infekcji. Dlatego wykazanie istotnego podwyższenia limfocytozy zawsze wymaga kontroli w celu upewnienia się, że jest to wyraz stałej tendencji do progresywnego zwiększania się liczby limfocytów, a nie zjawisko jednorazowe. Podobnie – powiększenie (nawet znaczne) węzłów chłonnych z powodu infekcji lub lokalnego stanu zapalnego – może być okresowe i z czasem ulec regresji.
- Znaczne lub szybko postępujące powiększenie węzłów chłonnych (> 5-6cm).
- Znaczne powiększenie śledziony, grożące jej pęknięciem.
- Szybkie narastanie limfocytozy krwi obwodowej (dla wartości powyżej 30 000/µl, wzrost limfocytów >50% w ciągu dwóch miesięcy lub ich podwojenie w ciągu <6 miesięcy).
- Utrzymująca się niedokrwistość (hemoglobina <10 g/dl) lub małopłytkowość (liczba płytek krwi <100 tys/l). Niedokrwistość lub małopłytkowość autoimmunolo-giczna nie reagująca na leczenie kortykosteroidami.
- Pojawienie się objawów ogólnych (gorączka, nocne poty, utrata wagi).
- Objawowe zajęcie narządów pozawęzłowych.
LECZENIE PRZEWLEKŁEJ BIAŁACZKI LIMFOCYTOWEJ
Podstawową formą leczenia PBL przez wiele lat była immunochemioterapia, a więc zastosowanie leków, które mają zniszczyć komórki nowotworowe lub zahamować ich namnażanie, w skojarzeniu z przeciwciałami monoklonalnymi. W ostatnich latach nastąpił ogromny przełom w leczeniu przewlekłej białaczki limfocytowej, zarejestrowane zostały nowoczesne leki celowane (ukierunkowane molekularnie), z których szczególne znaczenie mają te hamujące przekazywanie sygnałów z receptora limfocytu B czy zwiększające ilość komórek nowotworowych ulegających apoptozie. Wykazują one wysoką skuteczność w leczeniu PBL, w tym również u chorych z wysokim ryzykiem genetycznym, czyli obecnością delecji krótkiego ramienia chromosomu 17 (del17p) lub mutacji TP53, obecnością delecji długiego ramienia chromosomu 11 (del11q) i niezmutowanym statusem IGHV.
Jak już wspomnieliśmy, wybór optymalnego dla każdego chorego sposobu leczenia zależy od czynników ryzyka związanych z PBL (w tym genetycznych), od wieku chorego, jego stanu ogólnego, występowania chorób współistnie-ących, ale również – przynajmniej w części przypadków – od preferencji pacjenta.
Co to oznacza? Może zostać Ci zaproponowany wybór pomiędzy terapią ograniczoną w czasie, zwykle trwającą przez 1 – 2 lat, a leczeniem przewlekłym, prowadzonym w sposób ciągły. Biorąc pod uwagę nawrotowy charakter PBL, niezależnie od stosowanego leczenia, większość z pacjentów będzie leczona z wykorzystaniem wszystkich możliwości, więc tak naprawdę nie wybie-ramy, jak będziemy leczeni, ale w jakiej kolejności wolimy, by stosowano u nas poszczególne metody.
Przed podjęciem leczenia należy omówić także kwestie prokreacyjne u pacjentów w wieku reprodukcyjnym. Większość stosowanych terapii przeciwnowotworowych ma działanie teratogenne, czyli działa toksyczne na zarodek oraz płód, mogąc powodować wady w trakcie jego rozwoju. Z tego powodu w trakcie leczenia onkologicznego oraz w krótkim okresie po jego zakończeniu należy stosować skuteczną metodę antykoncepcji w każdej sytuacji w której pacjentka lub partnerka pacjenta są przed okresem menopauzy. Tak samo, u młodych pacjentów, przed podjęciem leczenia warto porozmawiać o zabezpieczeniu płodności.
IMMUNOCHEMIOTERAPIA
W immunochemioterapii wykorzystuje się połączenie chemioterapeutyków (cytostatyków) np. fludarabina, cyklofosfamid, bendamustyna, chlorambucyl z przeciwciałami monoklonalnymi – rytuksymab, obinutuzumab .
Mechanizm działania cytostatyków opiera się na zabijaniu szybko dzielących się komórek – często zarówno komórek nowotworowych jak i zdrowych. Brak wybiórczości działania wpływa na pojawianie się działań nie-pożądanych, takich jak np. zmniejszenie liczby granulocytów czy podrażnienie/zapalenie śluzówek. Należy w tym miejscu zwrócić także uwagę na możliwość odległych w czasie następstw, takich jak tendencje do długotrwałych cytopenii (zwłaszcza obniżenia liczby leukocytów czy płytek krwi) czy większą możliwość powstania wtórnych procesów nowotworowych.
Z kolei przeciwciała monoklonalne łączą się z antygenami (białkami) obecnymi na powierzchni komórek nowotworowych. W leczeniu PBL wykorzystywane są przeciwciała anty-CD20 przeciwko antygenowi obecnemu na limfocytach B (rytuksymab, obinutuzumab).
Rola immunochemioterapii, która do niedawna była podstawą leczenia PBL, obecnie znacznie się zmniejszyła. W pierwszej linii dopuszcza się ją tylko u młodych chorych, w dobrym stanie ogólnym, bez jakichkolwiek czynników ryzyka. W praktyce oznacza to wyłącznie pacjentów bez delecji 17p/mutacji TP53, z obecnością mutacji IGVH i bez współistniejących chorób. Wszyscy pozostali pacjenci powinni otrzymywać nowe terapie celowane.
LECZENIE CELOWANE (UKIERUNKOWANE MOLEKULARNIE)
1.INHIBITORY KINAZY TYROZYNOWEJ BRUTONA
AKALABRUTYNIB
w monoterapii lub w skojarzeniu z obinutuzumabem jest wskazany w leczeniu dorosłych pacjentów z nieleczoną wcześniej PBL; w monoterapii jest wskazany w leczeniu dorosłych pacjentów chorych na PBL, którzy wcześniej otrzymali co najmniej jedną terapię.
IBRUTYNIB
ZANUBRUTYNIB
w monoterapii jest wskazany w leczeniu u dorosłych pacjentów z przewlekłą białaczką limfocytową.
- w skojarzeniu z obinutuzumabem jest wskazany w leczeniu dorosłych pacjentów z uprzednio nieleczoną PBL;
- w skojarzeniu z rytuksymabem jest wskazany w leczeniu dorosłych pacjentów chorych na PBL, którzy zostali uprzednio poddani co najmniej jednej terapii;
- w monoterapii jest wskazany w leczeniu PBL: u dorosłych pacjentów z obecnością delecji w obszarze 17p lub mutacją TP53, u których leczenie inhibitorem szlaku sygnałowego receptora komórek B jest nieodpo-wiednie lub nie powiodło się oraz u dorosłych pacjentów bez delecji w obszarze 17p lub mutacji TP53, u których nie powiodła się zarówno immunochemioterapia, jak i leczenie inhibitorem szlaku sygnałowego receptora komórek B.
PRZESZCZEPIENIE KOMÓREK MACIERZYSTYCH SZPIKU
PROGRAM LEKOWY DLA PRZEWKLEKŁEJ BIAŁACZKI LIMFOCYTOWEJ
TERAPIE REFUNDOWANE W POLSCE W RAMACH PROGRAMU LEKOWEGO B.79
W 1 LINII LECZENIA PBL
Leki refundowane w leczeniu pacjentów z delecją 17p (del17p)/ mutacją w genie TP53 (mutTP53) lub niezmutowanym statusem IgHV
Nie jest kryterium decydującym o refundacji
Leki refundowane w leczeniu pacjentów z delecją 17p (del17p)/ mutacją w genie TP53 (mutTP53) lub niezmutowanym statusem IgHV
Nie jest kryterium decydującym o refundacji
Nie jest kryterium decydującym
o refundacji
Schemat refundowany w leczeniu pacjentów z klirensem kreatyniny (CrCL): > 30ml/min oraz < 70 ml/min lub liczbą punktów wg skali CIRS > 6
Nie jest kryterium decydującym
o refundacji
Nie jest kryterium decydującym
o refundacji
Nie jest kryterium decydującym
o refundacji
Nie jest kryterium decydującym
o refundacji
Nie jest kryterium decydującym
o refundacji
Lek refundowany u pacjentów z przeciwwskazaniami do rozpoczęcia leczenia z wykorzystaniem schematu FCR zdefiniowanymi jako:
a) wiek 65 lat i powyżej
ALBO
b) wiek 18-64 lat i obecność co najmniej jednego z poniższych parametrów:
- klirens kreatyniny (CrCl) ≥ 30 ml/min oraz < 70 ml/min
- lub liczba punktów wg skali CIRS > 6
- lub wystąpienie w ciągu ostatnich 2 lat ≥1 ciężkiej infekcji (wymagającej hospitalizacji lub pozajelitowej antybiotykoterapii) lub ≥ 3 infekcji (wymagających doustnej antybiotykoterapii) potwierdzonych w dokumentacji medycznej pacjenta
TERAPIE REFUNDOWANE W POLSCE W RAMACH PROGRAMU LEKOWEGO B.79
W KOLEJNYCH LINIACH LECZENIA PBL
stosowano uprzednio co najmniej jedną linię leczenia, bez względu
na status delecji 17p (del17p) / mutacji w genie TP53 (mutTP53)
stosowano uprzednio co najmniej jedną linię leczenia, bez względu
na status delecji 17p (del17p) / mutacji w genie TP53 (mutTP53)
stosowano uprzednio co najmniej jedną linię leczenia, bez względu
na status delecji 17p (del17p) / mutacji w genie TP53 (mutTP53)
stosowano uprzednio co najmniej jedną linię leczenia, bez względu
na status delecji 17p (del17p) / mutacji w genie TP53 (mutTP53)
niepowodzenie po leczeniu inhibitorem BTK, udokumentowana obecność delecji 17p (del17p) / mutacji w genie TP53 (mutTP53)
WYBRANE DZIAŁANIA NIEPOŻĄDANE
obserwowane podczas lub/i po leczeniu
Stosowane leki nigdy nie są obojętne dla organizmu, jednak zarejestrowane są tylko te leki, w których korzyść z ich zastosowania przewyższa ryzyko. A zatem podajemy je, by pomóc i leczyć, ale musimy być przygotowani na działania niepożądane. Dlatego do każdej terapii należy właściwie się przygotować, przestrzegać zaleceń oraz uważnie obserwować reakcje swojego organizmu. Obserwowane działania niepożądane należy bezwzględnie zgłaszać lekarzowi/personelowi medycznemu. Powikłania leczenia możemy podzielić na te występujące w trakcie stosowania terapii oraz na powikłania odległe w czasie. Więcej informacji znajdziesz w części B poradnika, tu podsumowano jedynie najważniejsze informacje.
NUDNOŚCI ORAZ WYMIOTY związane z chemioterapią
Jest to najczęstsze powikłanie towarzyszące intensywnej immunochemioterapii: w schematach stosowanych u chorych na PBL należą do rzadkości.
INFEKCJE
związane z niedoborami odporności wynikającymi z samej choroby (PBL to przecież choroba nowotworowa układu odpornościowego) i prowadzonego leczenia.
Przy klasycznej chemioterapii najwięcej powikłań infekcyjnych wiązało się z neutropenią, spadkiem liczby granulocytów (komórek odpowiedzialnych za I linię obrony organizmu przed infekcjami). Po/w trakcie stosowania leków ukierunkowanych molekularnie neutropenie obserwuje się rzadziej; za infekcje w większym stopniu od-powiada niemal całkowita eradykacja limfocytów B, które są ważnym elementem odpowiedzi humoralnej. Przy poważnych infekcjach na-leży zawsze rozważyć przerwanie/odrocznie terapii PBL.
Każdy chory z infekcją COVID-19 powinien być, w pierwszych dniach po stwierdzeniu dodatniego wyniku testu, leczony w sposób aktywny. Zaniechanie takiego postępowania może mieć nieodwracalne skutki, szczególnie u osób nie-zaszczepionych lub nieefektywnie zaszczepionych.
Limfocyty białaczkowe nie produkują białek odpornościowych i jednocześnie ograniczają produkcję limfocytów prawidłowych. Niezależnie od tego, na jakim etapie choroby pojawi się infekcja, u chorego na PBL zawsze należy traktować ją poważnie, liczyć się z jej cięższym przebiegiem.
REAKCJE UCZULENIOWE NA LEKI
Przykładem reakcji alergicznej może być wysypka, obrzęk skórny, przejściowy spadek lub wzrost ciśnienia tętniczego krwi, często objawy te mają charakter przemijający.
Szczególnie często reakcje alergiczne mogą wywoływać przeciwciała monoklonalne (rytuksymab, obinutuzumab). Wynika to ze specyficznej budowy tych leków: są przeciwciałami, czyli białkami, które mogą wywoływać reakcje alergiczne. Mogą wystąpić również reakcje alergiczne zagrażające zdrowiu i życia pacjentów, jak np. wstrząs anafilaktyczny. Z tego powodu pierwsze podanie tych leków, gdy ryzyko reakcji alergicznej jest największe, odbywa się zawsze w warunkach hospitalizacji, przynajmniej w dziennym ośrodku leczenia.
ZESPÓŁ ROZPADU GUZA
Zespół objawów związany z szybkim niszczeniem komórek nowotworowych w następstwie terapii nazywany jest zespołem rozpadu guza (TLS, z ang. tumor lysis syndrome).
Chociaż zawsze cieszy nas skuteczność leczenia, szczególnie u chorych z opornością, sama skala zjawiska może być poważnym problemem klinicznym. U części pacjentów obserwuje się jedynie nieprawidłowe wartości parametrów laboratoryjnych (takich jak stężenie potasu i kwasu moczowego we krwi); w ciężkich przypadkach może dojść do zaburzeń w czynności nerek, nieprawidłowej pracy serca lub zaburzeń neurologicznych, dlatego jeśli będzie taka potrzeba – podanie leku nastąpi w warunkach szpitalnych. Ryzyko TLS jest szczególnie wysokie w pierwszych dniach lub tygodniach leczenia wenetoklaksem.
W przypadku wysokiego ryzyka wystąpienia zespołu lizy guza istnieje konieczność hospitalizacji podczas rozpoczynania leczenia – co pozwala na całodobową obserwację pacjenta i podjęcie szybkich, właściwych reakcji.
Ze względu na możliwość wystąpienia zespołu lizy guza konieczna jest ocena pacjentów pod kątem ryzyka jego wystąpienia oraz odpowiednia profilaktyka. W jej ramach stosuje się nawadnianie chorego (w części przypadków podając płyny infuzyjne dożylnie) oraz leki zmniejszają-ce stężenie kwasu moczowego (allopurynol, rasburykaza). Pozwala to na przyspieszone usuwanie metabolitów z organizmu i zmniejsza ryzyko wystąpienia zaburzeń. Picie dużej ilości wody, co najmniej 1,5 do 2 litrów na dobę, pomaga w usuwaniu z organizmu produktów rozpadu komórek nowotworowych z moczem i zdecydowanie zmniejsza ryzyko TLS.
POWIKŁANIA HEMATOLOGICZNE
Powikłania hematologiczne takie jak neutropenia, niedokrwistość lub małopłytkowość, mogą powodować samoistne krwawienia, znaczący spadek odporności, a tym samym infekcje i gorączki. Dlatego koniecznie zapoznaj się z ich objawami oraz metodami ich leczenia.
ZABURZENIA FUNKCJI NARZĄDÓW WEWNĘTRZNYCH
W trakcie terapii przeciwnowotworowej możliwe jest uszkodzenie narządów wewnętrznych w tym np. ostre uszkodzenie nerek czy wątroby. Przeważnie są to sytuacje przejściowe, związane z wcześniejszym uszkodzeniem narządów, które przy przerwaniu leczenia ustępują. W części przypadków musimy jednak zredukować dawki lub wręcz zmienić stosowany schemat leczenia, dlatego o wszelkim nasileniu objawów z ich strony koniecznie poinformuj lekarza lub ośrodek prowadzący.
POWIKŁANIA ZAKRZEPOWO-ZATOROWE
Pod pojęciem choroby zakrzepowo-zatorowej kryje się zakrzepica żył kończyn dolnych oraz zatorowość płucna.
Zakrzepicy sprzyja unieruchomienie (stąd ryzyko zakrzepicy wzrasta u chorych ograniczających swoją codzienną aktywność fizyczną; jest szczególnie wysokie u chorych hospitalizowanych) czy utrudnienie odpływu krwi żylnej, związane np. z uciskiem naczynia przez powiększony węzeł chłonny.
Ponadto rozwojowi zakrzepicy sprzyjają zarówno choroby nowotworowe jak i leczenie przeciwnowotworowe. Z tego powodu bardzo ważne jest stosowanie profilaktyki przeciwzakrzepowej, jeżeli istnieją do niej wskazania. Każdy pacjent jest oceniany pod kątem możliwości rozwoju zakrzepicy i w zależności od indywidualnej sytuacji może być zalecane leczenie przeciwkrzepliwe. W ramach profilaktyki najczęściej wykorzystywane są heparyny drobnocząsteczkowe, które podawane są codziennie w formie podskórnych zastrzyków lub leki przeciwzakrzepowe w tabletkach.
- W przebiegu zakrzepicy żył kończyn dolnych, w obrębie żył podudzi, ud lub innych żył, tworzą się zakrzepy. Najczęściej towarzyszą temu dolegliwości miejscowe pod postacią ocieplenia w miejscu powstania zakrzepu, bólu oraz zaczerwienienia i obrzęku. W przypadku, jeżeli skrzeplina z żyły oderwie się, może się przemieścić do płuc, zatykając naczynia płuc, co skutkuje zatorowością płucną. Pamiętaj, jeżeli zauważysz takie objawy – zgłoś się pilnie do lekarza.
- Zatorowość płucna może przebiegać bez-objawowo, jednak masywna zatorowość płucna jest stanem zagrożenia życia. W razie nagłego pojawienia się duszności, bólu – w swoim charakterze przypominającego ból wieńcowy – czy objawów niewydolności krążenia, należy pilnie wezwać pogotowie ratunkowe, by dalsza diagnostyka i leczenie mogły odbywać się w warunkach Szpitalnego Oddziału Ratunkowego (SOR).
KARDIOTOKSYCZNOŚĆ
Niektóre ze stosowanych leków mogą wpływać na funkcjonowanie serca w trakcie leczenia, a czasem nawet doprowadzać do jego uszkodzenia. Klasycznym przykładem są antracykliny – cytostatyki stosowane w leczeniu chłoniaków o agresywnym przebiegu. U pacjentów chorych na PBL coraz powszechniej stosuje się inhibitory kinazy Brutona opisane wcześniej.
Ibrutynib – inhibitor I generacji może może powodować u części chorych migotanie przedsionków (zaburzenia rytmu serca). Inhibitory II generacji (akalabrutynib i zanubrutynib) są bardziej selektywne i choć w praktyce o wiele rzadziej powodują takie działania niepożądane, rekomenduje się monitoring, pod kątem kardiologicznych działań niepożądanych, wszystkich pacjentów leczonych inhibitorami kinazy Brutona.
ZABURZENIA ODPORNOŚCI
Jednym z najczęstszych powikłań samej choroby jak i jej leczenia są zaburzenia odporności.Dotyczą one blisko połowy pacjentów chorych na PBL. Może dojść do zakażeń oportunistycz-nych, czyli wywoływanych przez takie drobno-ustroje, które u zdrowych osób nie stwarzają zagrożenia. Typ zakażeń różni się w zależności od etapu choroby, a także od rodzaju leczenia otrzymywanego przez pacjenta.
Przykładowo, u pacjentów nieleczonych oraz u leczonych cytostatykami, najczęstszą manifestacją – jako konsekwencje obniżenia liczby granulocytów – są infekcje górnych dróg oddechowych czy zapalenia płuc o etiologii bakteryjnej. Z kolei u chorych stosujących leki ukierunkowane molekularnie czy immunoterapię, może częściej dochodzić do reaktywacji chorób wirusowych, np. nawroty półpaśca, czy wirusowego zapalenia wątroby typu B.
Ważnym elementem leczenia wspomagającego w PBL jest zapobieganie powikłaniom infekcyjnym. Z tego powodu u pacjentów regularnie wykonywana jest morfologia – pozwala ona wykryć stany neutropenii oraz właściwie na nie reagować.
U części pacjentów, w trakcie terapii ukierun-kowanych molekularnie, zaleca się przyjmo-wanie profilaktycznych leków przeciwinfekcyj-nych. Acyklowir jest lekiem przeciwwiruso-wym, zapobiegającym reaktywacji wirusa ospy oraz półpaśca. Połączenie sulfametoksazolu
i trimetoprimu (biseptol) wykorzystywane jest w profilaktyce zakażenia oportunistycznego Pneumocystis jiroveci.
W przebiegu PBL występuje również nieprawidłowa produkcja immunoglobulin (przeciwciał odpornościowych, czyli specyficznych białek wspomagających walkę z infekcjami). W przypadku znacznego obniżenia ich wartości możliwe jest ich uzupełnianie dożylne.
Istotne w zabezpieczeniu odporności u pacjentów chorych na chłoniaki, w tym przewlekłą białaczkę limfocytową, są szczepienia ochronne. Wiemy, że z jednej strony chorzy z upośledzeniem odporności gorzej odpowiadają na szczepienia, z drugiej – bardziej od zdrowych osób ich potrzebują.
Stąd wynikają rozszerzone wskazania do szczepienia chorych na PBL. Każdy z pacjentów powinien być zaszczepiony p/COVID-19 ze względu na ciężki przebieg infekcji, o ile dojdzie do niej w czasie leczenia PBL. Na początku pandemii COVID-19, gdy nie były dostępne szczepionki i skuteczne leki przeciwwirusowe, śmiertelność przekraczała 25%. Obecnie, u chorych stosujących się do zaleceń, udało się nam ją obniżyć 10-ciokrotnie.
Przed rozpoczęciem leczenia powinno się rozważyć szczepienie przeciwko Streptococcus pneumoniae (szczepienie „przeciw pneumokokom”) oraz Haemophilus influenzae typu B (szczepienie „przeciw HiB”). Warto również wykonywać regularne, coroczne szczepienia przeciwko grypie.
POWIKŁANIA AUTOIMMUNIZACYJNE
Powikłania autoimmunizacyjne są związane z zaburzeniami odporności w przebiegu PBL, jednak obejmują inny zakres objawów niż powikłania infekcyjne.
W wyniku reakcji autoimmunologicznych na-stępuje ukierunkowanie komórek odporno-ściowych przeciw komórkom własnym organizmu. Powikłania autoimmunizacyjne często towarzyszą lub są następstwem infekcji.
- Niedokrwistość autoimmunohemolityczna (AIHA)- jej przyczyną jest powstawanie przeciwciał opłaszczających czerwone krwinki, co prowadzi do ich zniszczenia. Ponieważ niedokrwistość w przebiegu PBL może również wynikać z upośledzonej produkcji erytrocytów, konieczne jest zróżnicowanie obu tych przyczyn.
W przypadku niedokrwistości autoimmunohemolitycznej w badaniach laboratoryjnych można zaobserwować spadek haptoglobiny, wzrost bilirubiny (jeżeli wzrost jest znaczny, prowadzi do żółtaczki) oraz dodatni bezpośredni test antyglobulinowy (BTA, odczyn Coombsa). W niedokrwistości autoimmunohemolitycznej stosuje się leki immunosupresyjne: w pierwszej kolejności są to glikokortykosteroidy, a w przypadku ich nieskuteczności wlewy immunoglobulin, cyklofosfamid, azatioprynę lub rytuksymab.
- Małopłytkowość immunologiczna (IT) –mechanizm podobny do niedokrwistości autoimmunohemolitycznej. Wytwarzane są w nim specyficzne przeciwciała skierowane przeciwko płytkom krwi, co powoduje ich niszczenie. W leczeniu małopłytkowości immunologicznej wykorzystuje się podobne leki jak w przypadku niedokrwistości autoimmunohemolitycznej: glikokortykosteroidy, immunoglobuliny lub rytuksymab. W przypadku nieskuteczności wymienione-go leczenia możliwe jest wykonanie zabiegu splenektomii, czyli usunięcia śledziony.
WAŻNE
kiedy skontaktować się z lekarzem
Poniżej wypisane zostały objawy, których nagłe pojawienie się wymaga skonsultowania z lekarzem (w przypadku mniejszego nasilenia może to być lekarz pierwszego kontaktu).
- objawy infekcji
- samoistne pojawienie się wybroczyn na śluzówkach czy skórze, krwawienia z nosa, błon śluzowych
- pojawienie się krwi w moczu czy w stolcu
- uczucie kołatania serca, ból w klatce piersiowej, nagła duszność
- zaburzenia widzenia, zaburzenia mowy, niedowłady
- pojawienie się zmian skórnych np. wysypki
- pojawienie się nowego, wyczuwalnego guza
- silne bóle brzucha, szczególnie z obecnością innych objawów, jak np. biegunka, wymioty
Z racji na możliwe interakcje leczenia przeciwnotoworowego z jedzeniem, suplementami diety czy ziołami, w trakcie leczenia należy bezwzględnie przestrzegać zaleceń żywieniowych oraz szczerze poinformować lekarza o ich stosowaniu.
ROZWINĘŁA SIĘ U MNIE INFEKCJA
gdzie mam się kierować?
Pierwszym krokiem powinien być natychmiastowy kontakt z lekarzem pierwszego kontaktu, czyli lekarzem rodzinnym (lub z lekarzem w ramach Nocnej i Świątecznej Opieki Medycznej w przypadku dni wolnych od pracy).
Lekarz może zlecić dodatkowe badania laboratoryjne jak np. morfologia, badanie wykładników stanu zapalnego czy badanie ogólne moczu oraz rozpocząć leczenie – może zaordynować antybiotykoterapię lub leki stymulujące produkcję krwinek odpornościowych w przypadku neutropenii.
Może również, na podstawie wywiadu, badania lub wyników badań podstawowych, zadecydować o konieczności hospitalizacji i skierować do szpitala. Część infekcji jest możliwa do opanowania w warunkach domowych i nie wymaga leczenia szpitalnego.
- Zawsze miej przy sobie dokumentację leczenia PBL i ostatnie wyniki.
- Należy wziąć pod uwagę możliwe interakcje z innymi lekami, stąd nie powinny być one zlecane bez konsultacji lekarza prowadzącego. W razie infekcji, której leczenie jest zawsze priorytetem, lekarz prowadzący decyduje o wstrzymaniu bądź kontynuowaniu leczenia PBL.
SYTUACJE SZCZEGÓLNE
OPORNOŚĆ CHOROBY NA LECZENIE
Rzadko, ale czasem dzieje się tak, że komórki nowotworowe będą broniły się przed zastosowanym leczeniem i wytwarzały mechanizmy oporności na terapię. Dochodzi wówczas do znaczącego zwiększenia dynamiki choroby, trudności w jej opanowaniu i tym samym pogorszenia przebiegu nowotworu, co wymaga intensyfikacji leczenia i staje się większym wyzwaniem dla pacjenta i lekarzy.
POURAZOWE LUB SAMOISTNE PĘKNIĘCIE ŚLEDZIONY
Powiększona śledziona jest jednym z powodów rozpoczęcia leczenia PBL. Powiększona śledziona, badalna poniżej łuku żebrowego, nie jest chroniona przez „zbroję”, jaką są żebra i ściana klatki piersiowej, stąd może łatwiej ulegać urazom prowadzącym do jej pęknięcia.
Samo powiększenie śledziony może być odczuwane jako uczucie pełności i wywoływać zespół objawów związanych z zaburzeniami czynnościowymi ze strony przewodu pokarmowego. Jej pęknięcie i związane z tym nagłe rozciągnięcie torebki (najczęściej dochodzi do tzw. podtorebkowego pęknięcia śledziony) związane jest z silnymi dolegliwościami bólowymi.
Rozpoznanie można potwierdzić wykonując ba-danie USG. Każde podejrzenie pęknięcia śle-dziony wymaga pilnej konsultacji chirurgicznej, przy czym transportując chorego do szpitala, powinniśmy unikać szybkiej jazdy i nagłych wstrząsów (rozciągnięta torebka hamuje krwawienie, jej pęknięcie prowadzi do niekontrolowanej utraty krwi i wstrząsu).
AUTORZY PORADNIKA
Marta Morawska
Urszula Gosik
Monika Długosz-Danecka
Wojciech Jurczak
Pełną treść poradnika znajdziesz tutaj:



