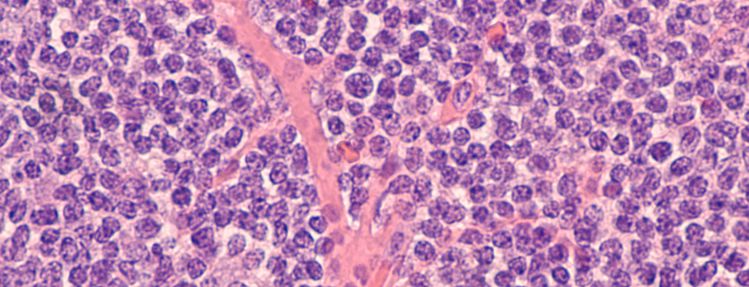
CHŁONIAK Z KOMÓREK PŁASZCZA
- ang. Mantle Cell Lymphoma
- międzynarodowy skrót: MCL
Chłoniak z komórek płaszcza (MCL, ang. Mantle Cell Lymphoma) jest nowotworową chorobą układu chłonnego. Prekursorem komórek nowotworowych są limfocyty B znajdujące się w strefie płaszcza, otaczającej grudkę chłonną. MCL należy do grupy chłoniaków o niepewnym rokowaniu.
Choroba, charakteryzuje się początkowo stosunkowo małą dynamiką podobnie jak w przypadku chłoniaków indolentnych (iNHL, ang. indolent Non-Hodgkin Lymphoma). Rokowanie i sposób leczenia MCL są jednak diametralnie różne, ze względu na stosunkowo wcześniej powstawanie oporności na immunochemioterapię, która może pojawić się już w pierwszej wznowie choroby. Podstawą leczenia MCL jest dążenie do uzyskania całkowitej odpowiedzi na leczenie, czyli remisji, przy czym pacjenci z remisją molekularną mają większe szanse na długie życie od tych, u których udało się osiągnąć jedynie remisję kliniczną. Ze względu na podobieństwo obrazu klinicznego MCL w pierwszym okresie choroby do chłoniaków indolentnych, ale tak różny sposób przebiegu choroby, niezmierne ważne i istotne jest u każdego pacjenta wykonanie badania histopatologicznego, przed podejmowaniem decyzji o leczeniu.
OBJAWY CHŁONIAKA Z KOMÓREK PŁASZCZA
Chociaż u większości chorych przy rozpoznaniu stwierdza się powiększone węzły chłonne, powiększoną śledzionę i zajęcie szpiku kostnego, pierwsze miesiące lub nawet lata mają przebieg skryty, skąpo-objawowy. Tzw. objawy ogólne (poty – zwłaszcza nocne, gorączki i znaczący spadek wagi ciała), czy zmiany w badaniu morfologii krwi obwodowej pojawiają się dopiero w późniejszym okresie, gdy mamy już organizmie większą masę komórek nowotworowych. W części przypadków komórki chłoniaka naciekają żołądek i jelita, co może powodować niespecyficzne zaburzenia czynnościowe ze strony przewodu pokarmowego (biegunki, wzdęcia, dolegliwości bólowe). Mogą być również zajęte migdałki, wtedy przy rozpoznaniu obraz przypomina niepoddającą się leczeniu antybiotykami „anginę” (zapalenie migdałków). Bardzo rzadko MCL rozpoznaje się w wycinkach ze spojówek.
DIAGNOSTYKA
Najczęściej chory zaniepokojony objawami ogólnymi wraz z ich nasileniem zgłasza się do lekarza I kontaktu. U chorych z podejrzeniem chłoniaka – w oparciu o wywiad lub wynik badania fizykalnego – lekarz powinien zlecić:
- podstawowe badania laboratoryjne (pobranie krwi: morfologia, badania czynności wątroby, czynności nerek)
- u wybranych chorych badania obrazowe (badanie ultrasonograficzne jamy brzusznej, miednicy i obwodowych węzłów chłonnych, RTG klatki piersiowej). W przypadku nieprawidłowego wyniku USG jamy brzusznej lub/i RTG klatki piersiowej powinien zlecić badanie tomograficzne, które pozwoli ustalić tzw. stopień zaawansowania klinicznego procesu chorobowego.
Jeśli badania wstępne wykażą nieprawidłowości, pacjent powinien zostać skierowany do hematologa, który kontynuuje proces diagnostyczny. Podstawowe znaczenie dla dalszej diagnostyki różnicowej ma decyzja o pobraniu materiału do badania histopatologicznego. U chorych z MCL może być to badanie trepanobioptyczne szpiku (wykonywane przez onkologów / hematologów) lub pobranie węzła chłonnego wykonywane przez chirurga na podstawie skierowania od hematologa lub lekarza I kontaktu. W wybranych przypadkach do rozpoznania wystarcza badanie krwi lub szpiku metodą cytometrii przepływowej.
Wynik badania histopatologicznego powinien zawierać niezbędny panel barwień immunohistochemicznych. Na wyniku powinno się znaleźć przynajmniej oznaczenie:
- antygenów występujących na limfocytach B (np. CD20 czy CD19),
- antygenu CD5, charakterystycznego dla limfocytów T
- cykliny D1.
Ponadto znaczenie prognostyczne ma obecność SOX11 (jej brak, może świadczyć o łagodnym przebiegu choroby i możliwości odroczenia leczenia) oraz wyrażona w % ekspresja ki67 (im wyższa, tym bardziej agresywny przebieg choroby).
Dodatkowym czynnikiem prognostycznym jest obecność dodatkowych zaburzeń cytogenetycznych, stąd ich badanie jest stałym elementem oceny chorych uczestniczących w badaniach klinicznych.
O rokowaniu, można się wstępnie wypowiedzieć korzystając z tzw. wskaźników (skal) prognostycznych -u chorych z MCL najczęściej stosuje się MIPI (ang. MIPI International Prognostic Index), uproszczony MIPI i tzw. „biologiczny MIPI”, jednak należy pamiętać, że uzyskany wynik określa jedynie prawdopodobieństwo przeżycia, a nie losy indywidualnego pacjenta. Wielu lekarzy pamięta chorych, którzy na przekór statystyce żyli długie lata, ciesząc się dobrym zdrowiem.
LECZENIE CHŁONIAKA Z KOMÓREK PŁASZCZA
W kolejnych paragrafach przedstawiono standard leczenia chłoniaka z komórek płaszcza, z podziałem na leczenie I linii oraz postępowanie w przypadkach nawrotowych / opornych. Metody leczenia których nazwy są w tekście w kolorze zielonym, są dostępne w ramach tzw. katalogu chemioterapii bez limitu. Metody z nazwami w kolorze żółtym, są dostępne jedynie w ramach tzw. programów terapeutycznych NFZ. Są jeszcze metody leczenia w ogóle nierefundowane przez NFZ – zaznaczone na kolor czerwony – dostępne OKRESOWO jedynie w badaniach klinicznych. Aktualna lista prowadzonych badań znajduje się TUTAJ.
ZIELONY
metody dostępne w ramach NFZ bez limitu
ŻÓŁTY
metody dostępne w ramach limitowanych programów terapeutycznych NFZ
CZERWONY
metody dostępne w ramach badań klinicznych lub niedostępne w Polsce
LECZENIE I LINII
Dotyczy to chorych z rozpoznaniem chłoniaka z komórek płaszcza, wcześniej nie leczonych
Decyzja o rozpoczęciu leczenia musi oznaczać jego konsekwentną kontynuację, ponieważ jego przedwczesne przerwanie zwiększa ryzyko pojawienia się oporności. Celem jest pozbycie się jak największej liczby komórek nowotworowych, tak by do wznowy choroby doszło jak najpóźniej. Oznacza to zastosowanie immuno-chemioterapii. U młodszych chorych, dobrze odpowiadających na leczenie stosujemy dodatkowo wysokodawkowaną chemioterapią wspomaganą autologicznym przeszczepieniem komórek macierzystych (ASCT ang. Autologous Stem Cell Transplantation). Każdy pacjent powinien być w następnych 2 latach poddany leczeniu podtrzymującemu z Rytuksymabem. Powodem tak konsekwentnego postępowania jest stosunkowo szybkie pojawianie się oporności na chemioterapię, najczęściej już w I wznowie choroby. Nadmierna ekspresja cykliny D1 oznacza bardzo głębokie zaburzenia cyklu podziału komórki, tak że szybko powstają wtórne, dodatkowe zaburzenia cytogenetyczne.
O samym wyborze immuno-chemioterapii I rzutu decyduje hemato-onkolog, w zależności od wieku chorego, stanu czynnościowego jego organizmu i chorób towarzyszących. U młodszych chorych podstawą chemioterapii są pośrednie dawki cytarabiny, zwykle podawane naprzemiennie z cyklami zawierającą antracykliny. Są to schematy R-CHOP/ R-HAD, R-CHOP/ R-DHAP czy podobne. U starszych pacjentów może być to sam R-CHOP, Rytuksymab z Bendamustyną lub wręcz R-CVP (pochodzenie schematów opisane jest szerzej w zakładce immuno-chemioterapia). Poddanie pacjenta konsolidacji z ASCT jest wyrazem naszej bezradności – przeszczep nie daje gwarancji wyleczenia choroby, wydłuża jednak istotnie czas do jej wznowy.
W ostatnich latach pojawiły się nowe metody leczenia, takie, jak inhibitory kinazy Brutona, które mają inny niż chemioterapia mechanizm działania. Zastosowanie ich w leczeniu I rzutu jest przedmiotem toczących się badań klinicznych. Nie znamy jeszcze ich wyniku, jednak prawie na pewno wydłużają one czas trwania odpowiedzi na leczenie. W całym procesie leczenia walczymy jednak finalnie o to, aby pacjent miał jak najdłuższy całkowity czas życia, stąd już w I linii leczenia inhibitorów BTK (obecnego standardu leczenia wznowy procesu) nie musi do tego prowadzić. I z myślą o takim rezultacie planowane jest leczenie i uwzględnienie konkretnych jego elementów.
LECZENIE WZNOWY / OPORNOŚCI NA LECZENIE I LINII
W momencie wystąpienia wznowy choroby lub oporności na leczenie I rzutu w NFZ jedyne, co lekarz może zaproponować, to alternatywne schematy immuno-chmioterapii. Im później po zakończeniu leczenia I rzutu dochodzi do wznowy procesu, tym większa nadzieja na ich skuteczność.
W Europie standardem postępowania we wznowie lub oporności jest leczenie z zastosowaniem wspomnianych już nowych leków. Od 2023 w katalogu chemioterapii pojawił się Lenalidomid (IMID, ang. immunomodulatory drugs), którego wyższość nad chemioterapią udowodniono w randomizowanych badaniach klinicznych III fazy, w których również braliśmy udział. Dostępne są już również inhibitory kinazy Brutona – ibrutynib– leki podawane w tabletkach, stosowane przewlekle – podobnie jak w leczeniu nadciśnienia tętniczego – do czasu pojawienia się oporności lub nietolerancji. Pierwsze badania, prowadzące do rejestracji Ibrutynibu przez Amerykańską Agencje Żywności i Leków (FDA, ang. Federal Drug Agency), prowadziliśmy w Krakowie już w 2010 roku. Aktualnie w Pratia MCM Kraków prowadzone są badania kliniczne z inhibitorami kinazy Brutona nowej generacji bądź ich stosowaniem w połączeniu z innymi lekami.
U chorych opornych na inhibitory kinazy Brutona, prowadzimy badania kliniczne z Wenetoklaksem, inhibitorami kinazy IP3 oraz nowymi inhibitorami kinazy Brutona przełamującymi oporność na leki I generacji oraz przeciwciałami bispecyficznymi.
W III linii w ramach programu lekowego dostępne jest leczenie CAR-T dla pacjentów, którzy w drugiej linii przeszli terapię ibrutynibem. Ponadto można we wznowie i oporności stosować alternatywne schematy immuno-chemioterapii. W wybranych przypadkach rozważa się allogeniczny przeszczep komórek hemopotycznych.
Chcesz wiedzieć więcej?
Nasze publikacje, wystąpienia na sesjach edukacyjnych i prezentacje wyników badań prowadzonych przez Zespół Leczenia Chłoniaków u chorych z MCL znajdą Państwo w Strefie Wiedzy.
Poznaj Autora:

prof. Wojciech Jurczak
Od 2007 roku zajmuje się prowadzeniem badań klinicznych we współpracy z Pratia – MCM Kraków, gdzie jako główny badacz i koordynator krajowy wziął udział w rejestracji 12 z 15 wprowadzonych w tym czasie na świecie innowacyjnych leków w terapii chłoniaków. Jest autorem i współautorem ponad 100 publikacji o zasięgu międzynarodowym. Jest konsultantem medycznym Europejskiej Agencji Leków (EMA).


