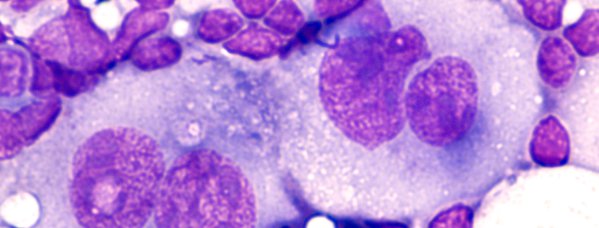
CHŁONIAK HODGKINA
- ang. Hodgkin Lymphoma
- międzynarodowy skrót: HL lub HD
Chłoniak Hodgkina, czasem opisywany jako choroba Hodgkina – dawna nazwa – ziarnica złośliwa – to nowotwór złośliwy układu chłonnego. Charakteryzuje się występowaniem nacieku zapalnego o zmiennym obrazie z niewielkim odsetkiem (1-2%) nowotworowych komórek wywodzących się linii limfocytów B – komórek Hodgkina i Reed-Sternberga.
Zanim zaczniesz czytać dalej…
Chwila, w której dowiadujesz się o rozpoznaniu choroby nowotworowej, jaką jest chłoniak Hodgkina, z pewnością wiąże się z szokiem. Pojawiają się obawy, niepewność i stres, dotychczasowe życie ulega zmianie, a plany na przyszłość wydają się trudne do realizacji. Na samym początku warto wiedzieć, że chłoniaki to odrębna grupa nowotworów, inna niż raki oraz mięsaki.
Chłoniak Hodgkina to zatem nowotwór, ale nie rak i jest w większości przypadków chorobą uleczalną.
WSTĘP
EPIDEMIOLOGIA
Chłoniak Hodgkina to stosunkowo rzadka choroba i stanowi zaledwie 0,5% nowotworów, a zachorowalność wynosi 2 na 100 tys osób rocznie. Chociaż choroba ta może wystąpić w każdym wieku, to przede wszystkim dotyka młodych dorosłych, a drugi szczyt zachorowań przypada po 55 r.ż. W Polsce chłoniak Hodgkina stanowi około 10% wszystkich chorób nowotworowych układu chłonnego.
Zarówno chłoniak Hodgkina, jak i chłoniak pierwotny śródpiersia, które rozpoznaje się stosunkowo często u osób młodych, mogą mieć podobny przebieg kliniczny z zajęciem węzłów chłonnych śródpiersia, przez co wymagają diagnostyki różnicującej jedną chorobę od drugiej. Jest to możliwe wyłącznie w oparciu o badanie histopatologiczne.
SKĄD SIĘ BIERZE?
Pochodzenie choroby nie jest do końca jasne i nie wiadomo, dlaczego dana osoba zachorowuje właśnie na chłoniaka Hodgkina. Chłoniaki rzadko mają tendencję tendecję do występowania rodzinnego, jednak nie mówimy o dziedziczeniu, a raczej o trudno uchwytnych czynnikach środowiskowych, takich jak zanieczyszczenia środowiska, styl życia i inne. Zdarza się to bardzo rzadko, dlatego nie ma szczególnej potrzeby planowania profilaktycznych badań u dzieci czy rodzeństwa pacjentów.
Wszystkie choroby nowotworowe, w tym chłoniaki, są częstsze u osób z zaburzeniami odporności (wrodzonymi lub nabytymi w przebiegu różnych chorób). Badania wskazują na trzykrotnie większe ryzyko za-chorowania na HL u osób zakażonych wirusem Epstein-Barr.
SKĄD WIADOMO, że to na pewno chłoniak Hodgkina?
Podstawowym i najważniejszym badaniem jest pobranie węzła chłonnego lub innej podejrzanej o zmiany nowotworowe tkanki. Dla szybkiej i prawidłowej diagnostyki niezmiernie ważne jest, aby pobrać cały węzeł lub przynajmniej fragment tkanki podejrzanej. Nie wystarczy biopsja cienkoigłowa (strzykawkowa), ponieważ w jej przypadku wynik może być fałszywie ujemny, a w sytuacji podejrzenia choroby, tak czy inaczej, najczęściej pacjent kierowany jest na pobranie węzła lub tkanki.
Pobrany materiał zostaje odpowiednio utrwalony i przesłany do pracowni histopatologicznej, gdzie po szeregu badań dodatkowych określa się, czy i jaki nowotwór się w nim znajduje. Ten proces może trwać nawet kilka tygodni.
Choć słysząc o podejrzeniu chłoniaka, chcielibyśmy, aby ostateczna diagnoza padła jak najszybciej, koniecznie należy uzbroić się w cierpliwość. Nawet przy szybkim terminie pobrania, trzeba poczekać na dokładną ocenę histologiczną, co może być dodatkowo opóźnione, jeżeli zakład patologii, w którym oceniane są wycinki, nie specjalizuje się w diagnostyce chłoniaków i po wstępnej ocenie przesyła je do ośrodka referencyjnego.
W przypadku chłoniaka Hodgkina odczekanie kilkunastu dodatkowych dni przeważnie nie ma większego znaczenia dla powodzenia leczenia: sama choroba toczy się u większości chorych od wielu miesięcy, a bardzo ważne jest ustalenie prawidłowej terapii w oparciu o ostateczny wynik histopatologiczny.
Są różne podtypy histologiczne chłoniaka Hodgkina. W zależności od tego, jak wyglądają i są ułożone komórki w nowotworze wyróżnia się cztery podtypy klasyczne, które jednak leczymy w identyczny sposób. Jest jednak także podtyp nieklasyczny chłoniaka Hodgkina, który choć nazywa się podobnie, należy do zupełnie odmiennej grupy chłoniaków – nazywanych indolennymi – i także jest leczony w odmienny sposób.
ROKOWANIE
Jak już wspomniano, chłoniak Hodgkina charakteryzuje się bardzo dobrym, jak na chorobę nowotworową, rokowaniem. Ponad 90% osób, które zachorują, wyleczy się całkowicie. Warto pamiętać, że wciąż pojawiają się nowe leki, które poprawiają szanse u osób z postacią oporną, czyli słabo reagującą na leczenie lub nawracającą, gdy musimy stosować kolejne linie leczenia.
OBJAWY CHŁONIAKA HODGKINA
JAK POSTĘPUJE CHOROBA
Często początkowo zajęte są węzły chłonne śródpiersia, których lekarz nie może stwierdzić nawet w dokładnym badaniu fizykalnym pacjenta. Początek może być skryty, skąpoobjawowy, stąd często choro-bę rozpoznaje się u osób ze stosunkowo dużą „masą guza”. Choroba może rozprzestrzeniać się do kolejnych węzłów chłonnych, wątroby, śledziony, może zajmować narządy pozawęzłowe i kości, natomiast zajęcie szpiku kostnego jest bardzo rzadkie.
Pierwszym sygnałem choroby może być wystąpienie objawów ogólnych (gorączka, poty nocne, niezamierzony spadek masy ciała) lub pojawienie się świądu skóry, często nieskutecznie leczonego przez dermatologa.
Podejrzenie choroby może się pojawić podczas standardowego badania lekarskiego lub z powodu znalezienia przez samego chorego powiększonego węzła chłonnego.
U co czwartego pacjenta (25% chorych) w chwili rozpoznania stwierdza się jeden lub więcej z poniższych objawów:
- niezamierzona utrata wagi,
- poty nocne wymagające zmiany bielizny,
- gorączki lub stany podgorączkowe,
- kaszel lub/i krwioplucie,
- świąd skóry,
- złe samopoczucie, głównie ból stawów po spożyciu alkoholu,
- osłabienie.
Trzeba pamiętać, że poza wyżej wy-mienionymi mogą pojawić się inne objawy spowodowane uszkodzeniem narządu, w którym rozwija się choroba, np. spadek tolerancji wysiłku i duszność wysiłkowa przy masywnym zajęciu śródpiersia
MAM DIAGNOZĘ i co dalej?
Kiedy już wiadomo, że chorujesz na chłoniaka Hodgkina, bardzo ważnym kolejnym krokiem jest ocena stanu zaawansowania choroby. Jednak musisz wiedzieć, że w chłoniakach o powodzeniu leczenia w większym stopniu decyduje odpowiedź na leczenie niż jego wyjściowe zaawansowanie. Stan zaawansowania potrzebny jest zatem nie tyle po to, by zobaczyć, jak późno została zdiagnozowana choroba, ale by prawidłowo dobrać intensywność leczenia.
Aby ocenić stan zaawansowania choroby, wykonuje się zwykle PET-TK. Jest to standardowe w tej chorobie badanie, które pokazuje jej zaawansowanie.
Ponadto lekarz zleci badania krwi takie jak:
- MORFOLOGIA Może być prawidłowa albo pojawia się podwyższona liczba białych krwinek, w tym granulocytów. Rzadziej dochodzi do zaburzeń płytek krwi, czerwonych krwinek lub obniżenia poziomu limfocytów w postaciach zaawansowanych.
- Kreatynina, mocznik i kwas moczowy jako parametry funkcji nerek.
- Transaminazy (AST i ALT), bilirubina, LDH, ALBUMINA jako ocena wydolności wątroby oraz oceny wskaźnika prognostycznego w postaciach zaawansowanych.
- Szukając informacji o tym chłoniaku, możesz spotkać się także z badaniem szpiku, tzw. trepanobiopsją. Obecnie, u chorych z wykonanym badaniem PET-TK, przy braku podejrzenia zajęcia szpiku, odstępuje się od tego badania.
STADIUM ZAAWANSOWANIA
Na podstawie wykonanych badań można ustalić stan zaawansowania choroby, używa się w tym celu międzynarodowego systemu. Do 2014 roku obowiązywała klasyfikacja z Ann Arbor w modyfikacji z Cotswold. Od 2014 roku do oceny zaawansowania choroby obowiązuje klasyfikacja z Lugano.
W chłoniakach nie mówimy o przerzutach, lecz o stadiach zaawansowania klinicznego. Leki, które stosujemy w leczeniu chłoniaków, podane dożylnie lub doustnie, działają w całym organizmie chorego, stąd III i IV stopień zaawansowania klinicznego nie musi oznaczać gorszego rokowania, a jedynie odmienne leczenie. Rokowanie zależy zatem głównie od wrażliwości choroby na leczenie, a nie od wyjściowego stadium zaawansowania.
CO DZIEJE SIĘ PRZED LECZENIEM
Chłoniaka Hodgkina leczy się głównie chemioterapią, czasem uzupełnioną o radioterapię. W przypadkach nawrotowych/opornych stosujemy dodatkowo tzw. „celowaną chemioterapię” (przeciwciała monoklonalne sprzężone z uwalnianą we wnętrzu komórki nowotworowej toksyną) i immunoterapię. Schemat leczenia ustala się po przeanalizowaniu stadium zaawansowania choroby, wieku, stanu ogólnego oraz chorób współistniejących. Dlatego ważne, aby lekarz prowadzący otrzymał wszelkie informacje na temat stanu zdrowia chorego i dolegliwości. Chodzi o to, by leczenie było nie tylko skuteczne, ale także bezpieczne. Kwestie – z pozoru błahe – mogą wpłynąć na wynik leczenia.
1. Przed rozpoczęciem leczenia należy pamiętać o wizycie u lekarza stomatologa. Trzeba upewnić się, czy nie ma ognisk zapalnych, które należy wyleczyć przed rozpoczęciem chemioterapii.
2. Szczepienia ochronne – choć w mniejszym stopniu – chronią pacjentów chorych na chłoniaki, również tych w trakcie chemioterapii. Należy omówić z lekarzem, które szczepionki są zalecane. U wszystkich chorych wskazane jest przeprowadzenie poniższych szczepień:
- p/grypie (sezonowo)
- p/ Streptococcus pneumoniae
- p/WZW B (zależnie od pozio-mu przeciwciał u pacjentów wcześniej szczepionych oraz u wszystkich niezaszczepionych)
- To także „czas najwyższy”, by zaszczepić się przeciwsko COVID-19, o ile już tego nie zrobiliśmy. Infekcja COVID-19, w czasie leczeia chłoniaka ma u niezaszczepionych osób szczególnie ciężki przebieg, u części chorych, może być przyczyną śmierci. We wszystkich przypadkach wymaga przerwania leczenia, co zmniejsza jego skuteczność lub wręcz prowadzi do powstania oporności.
W miarę możliwości szczepienia powinno się przeprowadzić do 2 tygodni przed planowaną terapią. Jeśli jednak się to nie uda, warto ustalić z lekarzem prowadzącym najdogodniejszy termin.
3. Przed rozpoczęciem leczenia, celem kwalifikacji, wskazana jest konsultacja kardiologiczna z oceną echokardiograficzną serca. W leczeniu I linii standardem są antracykliny, które są lekami potencjalnie kardiotoksycznymi.
4. Warto przedyskutować z lekarzem możliwości dotyczące zabezpieczenia płodności. Szczególnie w przypadku planowania bardziej intensywnej chemioterapii. Jednak trzeba pamiętać, że w rzadkich przypadkach oporności lub nawrotu choroby – w sposób nieplanowany – może być potrzebne szybkie wdrożenie intensywnego leczenia.
U kobiet leczenie onkologiczne ma zróżnicowany wpływ na płodność. Jest zależnie od: wieku pacjentki (mniejsza szkodliwość leczenia u pacjentek przed 30 rokiem życia, z wyższą wyjściową rezerwą jajnikową), zaawansowania choroby, zastosowanego leczenia (chemio- i radioterapia), dawki leków.
U mężczyzn wpływ terapii na płodność zależy od zaawansowania choroby oraz rodzaju leków i ich dawek. Nie ma natomiast znaczenia wiek pacjenta. Plemniki powstają wciąż na nowo, więc, po powrocie do zdrowia, ich pula może zostać odbudowana, jeśli tylko nie nastąpiło ciężkie i nieodwracalne uszkodzenie komórek, z których powstają plemniki.
LECZENIE I LINII
Po postawieniu rozpoznania, lekarz zaproponuje Ci odpowiednią chemioterapię. W przypadku chłoniaka Hodgkina jest to tak zwane leczenie radykalne i ma na celu całkowite wyleczenie choroby. Zależnie od stopnia zaawansowania oraz stanu ogólnego, zostanie wybrany jeden ze schematów leczenia. W przypadkach braku zadawalającej regresji zmian może być konieczne leczenie II linii, często z zastosowaniem celowanej lub wysokodawkowanej chemioterapii, o czym przeczytasz dalej.
CHOROBA OGRANICZONA
ABVD x 2
PET - TK
RADIOTERAPIA LUB KONTYNUACJA CHEMIOTERAPII
W przypadku ABVD – schematu stosowanego w mniej zaawansowanych postaciach choroby, leczenie odbywa się najczęściej ambulatoryjnie – w Oddziale Leczenia Dziennego, choć w dobie zwiększonego ryzyka zakażeń SARS-CoV-2 zależy to od indywidualnej organizacji ośrodka pro-wadzącego. Znajdujące się w tym schemacie cztery leki podawane są dożylnie, co dwa tygodnie. Jeden kurs to dwie takie wizyty, każdy kurs trwa więc 4 tygodnie.
W przypadkach bez dużej masy guza, czy nasilonych objawów ogólnych, z całkowitą regresją metaboliczną i dobrą odpowiedzią morfologiczną we wczesnej ocenie PET-CT po 2-gim cyklu leczenia, można zastosować radioterapię lub kontynuować chemioterapię (decyzje podejmowane są indywidualnie). U pozostałych Pacjentów najczęściej proponowanym standardem jest 6 cykli ABVD z następową, uzupełniającą radioterapią.
U części chorych z ograniczonym stadium zaawansowania klinicznego można rozważyć intensywniejsze schematy chemioterapii, co zwiększa prawdopodobieństwo pominięcia radioterapii, z którą wiążą się pewne powikłania odległe, w tym większe ryzyko wtórnych, występujących po 10-15 latach, procesów nowotworowych.
CHOROBA ZAAWANSOWANA
A+AVD x 2 lub ABVD x 2
lub ESKALOWANY BEACOPP x2
PET - TK
KONTYNUACJA CHEMIOTERAPII +/- RADIOTERAPIA
Chemioterapia A + AVD (AVD z brentuksymabem wedotyny) jest obecnie dostępna dla chorych na chłoniaka Hodgkina w IV stopniu zaawansowania w ramach programu lekowego. Badania kliniczne wykazują jej wyższą skuteczność w postaciach zaawansowanych niż klasycznego schematu ABVD.
Schemat BEACOPP jest opcją terapeutyczną dla pacjentów młodszych, bez istotnych chorób współistniejących. Jego stosowanie wymaga kilkudniowych pobytów w szpitalu.
Staramy się o uzupełnienie refundacji o schemat BRECADD, w którym brentuksymab wedotyny kojarzy się z intensywniejszą od AVD chemioterapią. Takie postępowanie pozwala u dobrze odpowiadających chorych na skrócenie leczenia, przy zachowaniu wysokiej skuteczności.
Po dwóch kursach chemioterapii wykonuje się badanie PET-TK. W razie uzyskania satysfakcjonujących wyników chemioterapię kontynuuje się zgodnie z pierwotnym planem. Lekarz może zaproponować w takiej sytuacji zmniejszenie intensywności niektórych schematów: ABVD do AVD oraz BEACOPP do ABVD.
Po zakończonej powodzeniem chemioterapii mogą pozostać tzw. aktywne zmiany resztkowe choroby i wówczas stosujemy uzupełniającą radioterapię.
JEŚLI POTRZEBNA JEST RADIOTERAPIA
Leczenie choroby opornej lub nawrotowej
Jeśli choroba nie poddaje się terapii lub powraca, trzeba opracować nowy plan mający na celu wyleczenie.
Pacjenci młodzi, bez poważnych chorób towarzyszących, poddawani są bardziej intensywnej chemioterapii (zwykle wymaga to pobytów w szpitalu), a następnie proponuje się im autologiczne przeszczepienie komórek macierzystych (ASCT).
W Polsce istnieje możliwość stosowania dwóch nowych leków zgodnie z wymogami programów lekowych, w ramach których są one dostępne. Pierwszym z nich jest brentuksymab wedotyny – przeciwciało skierowane przeciw antygenowi CD30, skojarzone z toksyną komórkową (wspomniana już wcześniej tzw. „celowana chemioterapia”). Mogą z niej skorzystać mogą pacjenci poddani wcześniej autologicznemu przeszczepieniu komórek macierzystych lub z opornością na przynajmniej 2 wcześniej stosowane schematy chemioterapii.
Drugi z leków to niwolumab (inhibitor punktu kontrolonego). Można go podawać po wcześniejszym zastosowaniu brentuksymabu wedotyny. Tak więc refundacja nowych leków u pacjentów z rozpoznaniem chłoniaka Hodgkina jest w Polsce stosunkowo dobra.
W połączeniu z dużym doświadczeniem ośrodków transplantologicznych, wyniki leczenia są w pełni porównywalne do innych, zamożniejszych krajów europejskich. Większym problemem pozostaje jedynie leczenie chłoniaka Hodgkina u osób starszych, po 60 roku życia, u których na wynik leczenia wpływa obecność chorób towarzyszących, ograniczając możliwość skutecznego wykorzystania chemioterapii.
GDY LECZENIE SIĘ ZAKOŃCZY
Po zakończonym leczeniu będziesz zgłaszać się do lekarza hematologa na wizyty kontrolne.
- Co 3 miesiące przez pierwsze pół roku.
- Co 6 miesięcy do 4 roku obserwacji.
- Następnie co rok.
Wynika to z faktu, że ryzyko nawrotu choroby jest najwyższe w pierwszych miesiącach od zakończenia terapii.
Na wizytach lekarz będzie z Tobą rozmawiał, badał Cię i oceniał wyniki badań krwi. Badania obrazowe (TK/PET-TK) wykonuje się tylko w przypadku podejrzenia nawrotu choroby.
DLACZEGO CZASEM POZOSTAJE ŚLAD PO CHOROBIE?
U pacjentów z dużą masą guza po leczeniu obserwujemy obecność tzw. zmiany rezydualnej, czyli tkanki włóknistej w miejscu pierwotnych nacieków komórek nowotworowych. W różnicowaniu aktywnej choroby pomocne znaczenie ma ba-danie PET-TK, jednak by mogło być one wiarygodne, musi być wykonane nie wcześniej, niż w 4 tygodnie po zakończeniu ostatniego cyklu chemioterapii i 3 miesiące po zakończeniu radioterapii.
Nie każda aktywna zmiana w PET-TK oznacza nawrót. Może to być stan zapalny lub np. efekt stosowanych w danym momencie leków. Najważniejsze jest czytanie wniosków, które powinny zawierać informację, czy dana zmiana jest podejrzana onkologicznie, czy nie, a przede wszystkim omówienie wyniku z lekarzem, który zna historię choroby. W sytuacji pojawienia się zmian niejednoznacznych, wątpliwych, zawsze należy rozważyć pobranie zmiany lub jej wycinka i weryfikację histopatologiczną.
AUTORZY PORADNIKA
Magdalena Olszewska-Szopa
Wojciech Jurczak
Pełną treść poradnika znajdziesz tutaj:



