
BIOSYMILARY
- ang. BIOSIMILAR MEDICINES
Biosymilary, zwane inaczej lekami biopodobnymi pełnią podobną rolę dla leków biologicznych co leki generyczne dla prostych cząsteczek. Po wygaśnięciu okresu ochrony patentowej (zwykle to 10 lat od momentu zarejestrowania leku), inne firmy farmaceutyczne mogą go wytwarzać.
W przypadku drobnych cząsteczek, sprawa jest prosta – należy dowieść, że produkt jest identyczny z pierwowzorem. Aspirynę zsyntetyzował w 1897 Felix Hoffmann, niemiecki chemik pracujący wówczas dla przedsiębiorstwa chemicznego Friedrich Bayer & Co (stąd znana starszym z Państwa nazwa „aspiryna bayerowska”), obecnie na rynku dostępne są prawie wyłącznie jej tańsze generyki.
Leki biologiczne, to o wiele bardziej skomplikowane cząsteczki peptydów lub białek, wytwarzane przez bakterie czy linie komórkowe. Przy zachowaniu identycznej sekwencji aminokwasów, każda wyprodukowana partia leku może różnić się nieznacznie, np. pod względem stopnia glikozylacji cząsteczki. Większe różnice mogą powstać przy zmianie linii produkcyjnej na nową czy rozpoczęciu wytwarzania leku w innym miejscu. Leki biopodobne są rejestrowane przez FDA (Amerykańską Agencje Leków i Żywności) i EMA (Europejską Agencję Leków) na podstawie rozbudowanej charakterystyki analitycznej cząsteczki oraz dodatkowo przeprowadzonych, specjalnie zaprojektowanych badań klinicznych. Daje to gwarancje bezpieczeństwa w pełni porównywalnej skuteczności klinicznej.
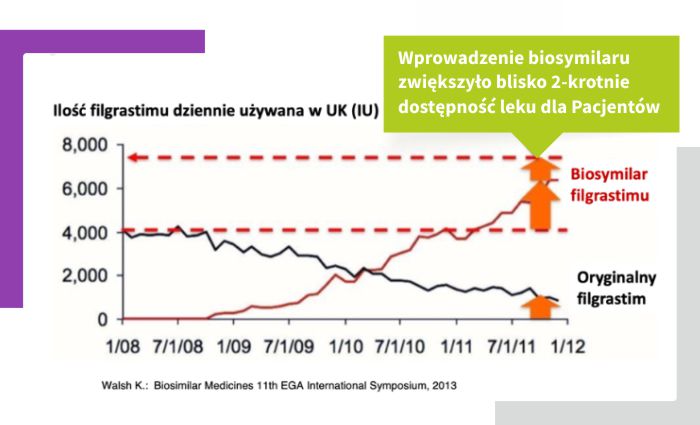
Chcesz wiedzieć więcej?
Zespół Leczenia Chłoniaków inspirował i prowadził badania rejestracyjne nad dwoma biosymilarami rytuksymabu zaaprobowanymi w Europie. W Państwach, gdzie je wprowadzono doprowadziło to do ponad 30% obniżki cen przeciwciał. Pierwsze przeciwciało biopodobne do rytuksymabu znalazło się na listach refundacyjnych we wrześniu 2019. W skali Polski szacuje się, że roczne oszczędności związane ze spadkiem ceny rytuksymabu przekroczą 80 milionów PLN.
Zespół Leczenia Chłoniaków w Pratia – MCM uczestniczył w badaniach, które doprowadziły do rejestracji biosymilarów rytuksymabu przez EMA i FDA. Publikacje znajdziesz w Strefie Wiedzy.


